Professional Documents
Culture Documents
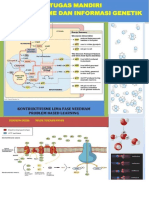
Biosintesis Asam Amino 2
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Biosintesis Asam Amino 2
Copyright:
Available Formats
Melati Fusvitasari (1004015159) Kelas 4H BIOKIM
Asam amino adalah prekursor dalam biosintesis nukleotida.
Asam amino berhubungan satu sama lain : keduanya adalah unit dasar di dalam biokimiawi penurunan sifat genetik Lintas biosintetik yang menghasilkan ke-20 jenis asam amino protein dan 8 nukleotida asam nukleotida asam nukleat,tidak hanya banyak jumlahnya tetapi juga kebanyakan bersifat agak kompleks. Masing-masing asam amino dibutuhkan dalam jumlah relatif kecil pada aliran biosintetik yang menghasilkan karbohidrat atau lemak pada jaringan hewan. Sebaliknya, karena asam amino yang berbeda harus dibuat dalam rasio yang benar dan pada waktu yang tepat untuk sintesis protein, lintas biosintetiknya harus diatur dan dikoordinasi satu sama lain.
Seperti halnya lintas metabolik lainnya jalur
biosintesis asam amino tidak sama jalurnya dengan degradasi.hubungan lintas biosintetik dan lintas kabolik diatur secara terpisah. lintas biosintetik menuju asam amino dan nukleotida sering dibahas bersama-sama. Kedua macam biomolekul tersebut mengandung atom nitrogen,yang berasal dari sumber-sumber biologis yang sama.
Terdapat 2 jenis asam amino berdasarkan kemampuan
tubuh dalam sintesisnya, yaitu asam amino esensial dan asam amino non esensial. Asam amino esensial adalah asam amino yang tidak dapat disintesis didalam tubuh,tetapi diperoleh dari luar misalnya melalui makanan (lisin, leusin, isoleusin,treonin, metionin, valin, fenilalanin, histidin, dan arginin). Asam amino nonesensial adalah asam amino yang dapat disintesis didalam tubuh melalui perombakan senyawa lain.
Nonesensial
Glutamat
glutamin prolin aspartat asparagin glisin serin sistein
Esensial Isoleusin Leusin Lisin Metionin
Fenilalanin
Treonin Triptofan Valin Arginin* Histidin
Makhluk hidup berbeda dalam kemampuannya
melakukan sintesis ke-20 macam asam amino. Juga berbeda dalam hal bentuk nitrogen yang dapat digunakan sebagai prekursor gugus amino. Sebagai contoh, tikus albino dan manusia hanya dapat melakukan sintetis 10 dari 20 asam amino yang dibutuhkan sebagai unit pembangun bagi biosintesis protein. Kesepuluh asam amino ini disebut Asam amino nonesensial atau asam amino yang dapat diganti,yang dibentuk dari ammonia dan berbagai sumber karbon.
Kesepuluh asam amino yang lain harus diperoleh dari
makanan dan karenanya disebut Nutritif asensial atau asam amino yang tidak dapat diganti. Tumbuhan tingkat tinggi lebih beragam, golongan tingkat ini dapat membuat semua asam amino yang dibutuhkan untuk sintesis protein.lebih lanjut,organisme tersebut dapat menggunakan baik amino maupun nitrat sebagai prekusor gugus amino. Sebagai contoh, Escherichia coli dapat membuat semua asam amino yang dibutuhkan untuk sintesis protein dari prekusor sederhana, tetapi bakteri asam laktat tidak dapat dan harus memperoleh asam amino tertentu dari lingkungannya.
1. Glutamat , Glutamin dan Prolin Mengambil Bagian dalam Lintas Biosintetik Bersama Dalam banyak hal prekursor tulang punggung asam amino nonesensial adalah asam -ketonya,yang pada akhirnya berasal dari senyawa antara siklus asam sitrat.gugus amino biasanya dilengkapi dengan reaksi transminasi dari glutamate, dikatalis oleh transminase, yang mengandung piridoksal fosfat sebagai gugus prostestetik. Lintas biosintetik menuju hubungan asam amino glutamat,glutamin dan prolin adalah sederhana dan napaknya identik dengan semua bentuk kehidupannya. Glutamate dibentuk dari ammonia -ketoglutarat,suatu senyawa antara siklus asam sitrat melalui kerja L-glutamat dehidrogenase. Tenaga pereduksi yang diperlukan diberikan oleh NADHP
NH4 + -ketoglutarat + NADHP <=> L-glutamat + +
H2O Reaksi ini adalah dasar yang penting didalam biosintesis semua asam amino, karena glutamate adalah donor gugus amino dalam biosintesis asam amino yang lain melalui reaksi transminasi. Lglutamat dehidrogenase terletak didalam matriks mitokondrion. Glutamin dibentuk dari glutamat melalui kerja glutamine sintetase Glutamat + NH4+ + ATP glutamin + ADP + Pi + H+
Pada kebanyakan organisme , asam amino nonesensial
alanin dan aspartat berturut-turut oleh berasal dari piruvat dan oksaloasetat oleh transaminasi dari glutamate.
Glutamate + piruvat <=> -ketoglutarat + alanin
Glutamate + oksaloasetat <=> -ketoglutarat + aspartat
Dalam banyak bakteri, aspartat adalah prekursor langsung
asparagin dalam suatu reaksi yang dikatalis oleh asparagin sintetase, analog dengan reaksi glutamine sintetase.tetapi pada mamalia ada perbedaan lintas untuk sintesis asparagin : gugus amino dipindahkan dari gugus amida glutamine menjadi gugus -karboksil aspartat oleh asparagin sintetase (bergantung ATP).
Untuk biosintesis Alanin, alanin dipindahkan ke sirkulasi
oleh berbagai jaringan, tetapi umumnyaoleh otot. Alanin dibentuk dari piruvat. Hati mengakumulasi alanin plasma,kebalikan transaminasi yang terjadi di otot dan secara proporsional meningkatkan produksi urea. Alanin dipindahkan dari otot ke hati bersamaan dengan transportasi glukosa dari hati kembali ke otot. Proses ini dinamakan siklusglukosa-alanin. Fitur kunci dari siklus ini adalah bahwa dalam 1 molekul, alanin.jaringan perifer mengekspor piruvat dan amonia ke hati, di mana rangka karbondidaur ulang dan mayoritas nitrogen dieliminir. Ada 2 jalur utama untuk memproduksi alanin otot yaitu: 1. Secara langsung melalui degradasi protein 2. Melalui transaminasi piruvat dengan bantuan enzim alanin transaminase,ALT (juga dikenal sebagai serum glutamat-piruvat transaminase, SGPT).
Tirosin adalah asam amino nonesensial, tetapi dibuat
oleh hewan dari asam amino esensial fenilanin melalui hidroksilasi pada posisi 4 pada gugus fenil oleh Fenilanin oksigenase, yang juga ikut serta dalam degradasi fenilalanin. Dalam reaksi ini NADPH dibutuhkan sebagai kopereduksi molekul oksigen ; dan mengingat kembali bahwa fenilalanin oksigenase adalah suatu monooksigenase atau oksidase berfunggsi ganda, reaksi yang dikatalis adalah : Fenilalanin + NADPH + H+ + O2 tirosin + + H2O
Pada mamalia , sistein dibuat dari dua asam amino lainnya,
metionin yang esensial didalam makanan dan serin yang tidak esensial. Metionin memberikan atom sulfur dan serin memberikan kerangka karbon pada sintesis sistein. Pada reaksi pertama didalam lintas ini, metionin diubah menjadi Sadenosilmetionin oleh reaksi ATP. Gugus adenosil dapat dianggap sebagai pembawa molekul metionin. Dalam bentuk ini,gugus metil pada metionin bersifat sangat reaktif dan dapat dipindahkan secara enzimatik ke berbagai senyawa penerima gugus metil , meninggalkan Sadenosilhomosistein sebagai produk demetilasi.
S-adenosilmetionin + penerima gugus metil S-
adenosilhomosistein + penerima termetilasi
Karena serin adalah precursor glisin, jalur biosintetik kedua asam
amino ini dianggap terjadi bersama-sama. Jalur utama bagi pembentukan serin didalam jaringan hewan dimulai dengan 3fosfogliserat, suatu senyawa antara glikolisis.pada tahap pertama, gugus -hidroksilnya dioksidasi oleh , menghasilkan 3fosfohidroksipiruvat. Transminase dari glutamate menghasilkan 3fosfoserin, yang mengalami hidrolisis oleh fosfoserinfosfatase , menghasilkan serin bebas. Asam amino serin dengan 3-karbon adalah prekursor glisin berkarbon 2, melalui penarikan satu atom karbon, pada posisi atau 3 reaksi dilangsungkan oleh enzim yang memerlukan koenzim tetrahidrofolat, yang merupakan bentuk aktif vitamin asam folat. Tetrahidrofolat adalah senyawa penerima atom karbon dari serin pada pemecahannya menjadi glisin. Atom karbon yang dipindahkan dari serin membentuk suatu jembatan metilen diantara atom nitrogen 5 dan 10 pada tetrahidrofolat, menghasilkan , 3-metilentetrahidrofolat. Reaksi keseluruhan, yang bersifat dapat balik adalah : Serin + tetrahidrofolat glisin + N5 , N10-metilentetrahidrofolat + H2O
Reaksi melengkapi pembentukan glisin dari serin. N5 , N10 -metilentetrahidrofolat adalah anggota
kelompok koenzim asam folat, yang mampu bersamasama dengan S-adenosilmetionin dan koenzim B12 , membawa berbagai jenis gugus 1-karbon ; unit 1karbon yang berasal dari serin dan dibawa oleh tetrahidrofolat dapat dipindahkan keberbagai molekul penerima. Pada hati vertebrata, glisin dapat dibuat melalui jalur lain yang dikatalis oleh enzim glisin sintase.
CO2 + NH4+ + NADH + + N5 , N10-metilentetrahidrofolat glisin + + tetrahidrofolat.
Untuk sebagian besar, tumbuhan dan mikroorganisme
yang hidup bebas membuat ini. Fakta bahwa manusia tidak dapat mensintesis mereka kecuali oleh protein merendahkan memiliki konsekuensi praktis. Setiap asam amino tunggal dapat membatasi dalam makanan. Jadi, misalnya, seorang individu yang tidak mendapatkan cukup tryptophan dalam diet tidak dapat mengkompensasi dengan makan lebih banyak metionin. Satu-satunya cara untuk mendapatkan tryptophan yang cukup akan memecah otot untuk melepaskan cukup triptofan untuk mendukung kehidupan. Ini berarti bahwa seseorang dapat benar-benar mati kelaparan sementara mendapatkan apa yang tampaknya menjadi cukup kalori dan protein
Lintas asam amino esensial yang paling kompleks
adalah lintas menuju fenilalanin,triptofan dan histidin yang memiliki cincin benzene atau heterosiklik. Sintesis cincin ini, terutama kedua cincin pusat triptofan, memerlukan sejumlah tahap enzimatis yang kompleks. Lima asam amino esensial bagi hewan disintesis oleh tanaman danmikroorganisme dari asam amino nonesensial :treonin, metionin dan lisin dibentuk dari aspartat, arginin dan histidin dibentuk dari glutamate. Isoleusin dibentuk olehbakteri dari asam amino esensial treonin Biosintesis isoleusin dari treonin.
Pengontrolan sintesis asam amino yang paling resfonsif adalah melalui
penghambatan alosterik reaksi pertama didalam urutan biosintetik oleh produk akhirnya. Reaksi pertama pada urutan tersebut yang biasanya bersifat tidak dapat balik, dikatalisis oleh suatu enzim alosterik. Contohnya yaitu rangkaian pengontrolan alosterik yang demikian teratur terhadap aktivitas glutamine sintetase E.coli . pada bakteri ini, glutamine adalah senyawa pemberi gugus amino pada biosintetis berbagai produk metabolic. Delapan produk metabolism glutamine pada E.coli sekarang diketahui bertindak sebagai modulator umpan balik negative terhadapa aktivitas glutamine sintetase,yaitu salah satu enzim pengatur yang paling rumit antara golongan enzim-enzim yang pernah kita ketahui. Karena 20-asam amino harus diproduksi dalam proporsi yang benar untuk melangsungkan sintesis protein. Sel telah mengembangkan bukan hanya caracara pengontrolan kecepatan sintesis asam amino itu secara sendiri-sendiri. Tetapi juga dengan cara mengkoordinasikan pembentukannya. Koordinasi tersebut,terutama berkembang dengan baik pada sel bakteri dalam kedaan tumbuh cepat. Memperlihatkan bagaimana sel E.Coli melakukan koordinasi sintesis asam amino lisin,mentionin,treonin,dan isoleusin,semuanya dibuat dari aspartat.
Jaringan yang saling berangkaian pada mekanisme
pengaturan di dalam biosintesis beberapa asam amino yang diturunkan dari aspartat pada E. coli.
Selain dari peranannya sebagai unit pembangunan protein,
asam amino adalah sejumlah biomolekul khusus, termasuk berbagai hormone, vitamin koenzim, alkaloid apolimer dinding sel, porfirin, antibiotik, pigmen dan senyawa neurotransmitter,semuanya memainkan peranan biologis penting. Contoh pertama adalah sintesis keratin, yang penting dalam bioenergetika otot dan syaraf, dalam bentuk fosfokreatin.Keratin dibuat dari tiga asam amino yaitu glisin, arginin, dan metionin.
TERIMA KASIH
You might also like
- BIOSINTESIS ASAM AMINODocument12 pagesBIOSINTESIS ASAM AMINORahma adila putriNo ratings yet
- Soal Asam NukleatDocument1 pageSoal Asam NukleathafiNo ratings yet
- Daftar Lengkap Asam Amino Esensial Dan Non EsensialDocument11 pagesDaftar Lengkap Asam Amino Esensial Dan Non EsensialpikaNo ratings yet
- Fenil PropanoidDocument7 pagesFenil PropanoidWigeSudirman100% (1)
- Asam Amino, Peptida Dan ProteinDocument36 pagesAsam Amino, Peptida Dan ProteinNurhayati SihombingNo ratings yet
- Bab 6 13 C NMR SpektroskopiDocument12 pagesBab 6 13 C NMR SpektroskopiSurya FatmadewiNo ratings yet
- Dasar Teori Asam AminoDocument3 pagesDasar Teori Asam AminoArya Mega UtamiNo ratings yet
- Penggolongan Senyawa MakromolekulDocument9 pagesPenggolongan Senyawa Makromolekuladhitya rizky SNo ratings yet
- Identifikasi Ion LogamDocument5 pagesIdentifikasi Ion LogamLailysakinatul AfiddahNo ratings yet
- Asam Amino Dan Protein BiokimiaDocument19 pagesAsam Amino Dan Protein BiokimiaAizIceNo ratings yet
- Asam Amino Dan ProteinDocument40 pagesAsam Amino Dan ProteinBrandon BuckleyNo ratings yet
- Makalah Kimor Organologam BaityDocument17 pagesMakalah Kimor Organologam Baityfebrina100% (1)
- Asam Amino Dan ProteinDocument28 pagesAsam Amino Dan ProteinMuhammad Abdur RokhimNo ratings yet
- Penentuan Kadar ProteinDocument29 pagesPenentuan Kadar ProteinKhudrotunnada AdityaNo ratings yet
- OPTIMALKAN KADAR PROTEINDocument17 pagesOPTIMALKAN KADAR PROTEINEka Andipa SuryanadaNo ratings yet
- Pengertian Senyawa OrganikDocument10 pagesPengertian Senyawa OrganikEMA LOVETA SARINo ratings yet
- Anabolisme ProteinDocument21 pagesAnabolisme ProteinFarmasi A 2018No ratings yet
- KumarinDocument19 pagesKumarinAthara SomanaNo ratings yet
- Bagian VI Struktur Tiga Dimensi ProteinDocument35 pagesBagian VI Struktur Tiga Dimensi ProteinmarfuzahNo ratings yet
- Kuliah 5. Biosintesis Asam LemakDocument52 pagesKuliah 5. Biosintesis Asam LemakMartunis RöFh100% (2)
- Redoks Kim2 1 PDFDocument3 pagesRedoks Kim2 1 PDFSenia Blessy PorajowNo ratings yet
- MONOTERPENADocument15 pagesMONOTERPENAVira Tyazs100% (1)
- Biosintesis Purin & PirimidinDocument28 pagesBiosintesis Purin & PirimidinNurse RoelNo ratings yet
- Titrasi KompleksometriDocument58 pagesTitrasi KompleksometriMuhammad Rizki ArdiansyahNo ratings yet
- AMINADocument43 pagesAMINALia Alwiah100% (3)
- Isolasi ArilbenzofuranDocument18 pagesIsolasi Arilbenzofuranleny_irawatiNo ratings yet
- Biokimia (Protein)Document18 pagesBiokimia (Protein)ratnawati100% (11)
- Senyawa HeterosiklikDocument33 pagesSenyawa HeterosiklikAyu Dwi Rahayu100% (1)
- TANIN DARI DAUN JAMBU BIJIDocument9 pagesTANIN DARI DAUN JAMBU BIJIJanghe Firmansyah Knc Tasik100% (2)
- MonoterpenDocument1 pageMonoterpenNur AvinaNo ratings yet
- Pengendalian Ekspresi GenDocument20 pagesPengendalian Ekspresi GenA. Dian MutmainnahNo ratings yet
- Critical Book Report Elektrokimia: Metode Kolorimetri"Document20 pagesCritical Book Report Elektrokimia: Metode Kolorimetri"Anonymous xqvxeUzNo ratings yet
- " Insulin ": Produksi Protein TerapeutikDocument18 pages" Insulin ": Produksi Protein Terapeutikika nur masrurohNo ratings yet
- Analisa Dan Identifikasi Kation Golongan 3 RevisiDocument7 pagesAnalisa Dan Identifikasi Kation Golongan 3 RevisiRaihanMuktiRamadhanNo ratings yet
- Andre Agasi S.L - 1022020016 - KimiaDocument10 pagesAndre Agasi S.L - 1022020016 - KimiaAndreNo ratings yet
- Biokimia ProteinDocument9 pagesBiokimia ProteinKanti Rahmi FauziyahNo ratings yet
- Pembahasan Penetapan Kadar Asam Amino Dengan Titrasi Formo1Document3 pagesPembahasan Penetapan Kadar Asam Amino Dengan Titrasi Formo1akubukanupitNo ratings yet
- BAB I PENDAHULUANDocument19 pagesBAB I PENDAHULUANCacaCizhukhaNo ratings yet
- Reaksi Amonia Dengan Alkil HalidaDocument6 pagesReaksi Amonia Dengan Alkil HalidaCitra Chairunnisa AzizNo ratings yet
- Power Point Kelompok 1 LiganDocument12 pagesPower Point Kelompok 1 LiganSilvia Wulandari100% (1)
- OPTIMASI ENZIMDocument10 pagesOPTIMASI ENZIMلوغيتفيكافوزيةNo ratings yet
- Tahap Proses Replikasi DNADocument5 pagesTahap Proses Replikasi DNAHaryani KesumaNo ratings yet
- DiskoneksiDocument27 pagesDiskoneksiFina RepitiyanaNo ratings yet
- DERET ASAM AMINODocument8 pagesDERET ASAM AMINOsilvia damayantiNo ratings yet
- Laporan Asam Amino Dan ProteinDocument26 pagesLaporan Asam Amino Dan ProteinReynaldi SaifulNo ratings yet
- Makalah Sinyal Dan Transduksi SinyalDocument8 pagesMakalah Sinyal Dan Transduksi SinyalDhimas Reyhan Putra SayudhaNo ratings yet
- Elektroforesis KapilerDocument6 pagesElektroforesis KapilerZepHemaNo ratings yet
- ALKALOIDDocument25 pagesALKALOIDkimiaexchange14No ratings yet
- Materi Uas BiokimiaDocument12 pagesMateri Uas BiokimiaLilis Eka HerdianaNo ratings yet
- 7 - (44) Alkohol, Fenol, Dan Tiol (Baru)Document44 pages7 - (44) Alkohol, Fenol, Dan Tiol (Baru)n420% (1)
- Asam Amino-Bms-1-12Document50 pagesAsam Amino-Bms-1-12odiliajessicanpviaNo ratings yet
- Makalah Asam Amino Dan ProteinDocument33 pagesMakalah Asam Amino Dan ProteinAsti Fiandari100% (1)
- Produksi RadionuklidaDocument4 pagesProduksi RadionuklidaBa'ist KhaerulNo ratings yet
- AminaDocument14 pagesAminaIntanNo ratings yet
- Asam Nukleat Dari Biologi Molekul Penting Bagi KehidupanDocument4 pagesAsam Nukleat Dari Biologi Molekul Penting Bagi KehidupanFaraditha AmaliaNo ratings yet
- Laporan Praktikum Analisis FisikokimiaDocument19 pagesLaporan Praktikum Analisis FisikokimiaElfa Ardi EffendiNo ratings yet
- Metabolisme ProteinDocument16 pagesMetabolisme ProteiniqbalNo ratings yet
- Adinda Asmaraputri 061011820225001 Kelas A Indralaya Tugas 7 MeingDocument27 pagesAdinda Asmaraputri 061011820225001 Kelas A Indralaya Tugas 7 MeingAdinda AsmaraputriNo ratings yet
- Metabolisme Asam AminoDocument16 pagesMetabolisme Asam AminoFitria MiftasaniNo ratings yet
- Metabolisme dan Katabolisme Asam AminoDocument13 pagesMetabolisme dan Katabolisme Asam AminoMuhammad YunusNo ratings yet
- Pidato Perpisahan Apoteker Uhamka XxviDocument2 pagesPidato Perpisahan Apoteker Uhamka Xxviapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Jurnal Ilmiah Kefarmasian: Evaluasi Penggunaan Antibiotik Berdasar Kriteria Gyssens Pasien Rawat Inap Di Departemen Ilmu Kesehatan Anak Rspad Gatot Soebroto Periode Juli - Desember 2014Document11 pagesJurnal Ilmiah Kefarmasian: Evaluasi Penggunaan Antibiotik Berdasar Kriteria Gyssens Pasien Rawat Inap Di Departemen Ilmu Kesehatan Anak Rspad Gatot Soebroto Periode Juli - Desember 2014apt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLP100% (2)
- Hitman SystemDocument395 pagesHitman Systemapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLP100% (3)
- 10 AntiepilepsiDocument12 pages10 Antiepilepsiapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Obat Lambung (Gi & Tukak Lambung)Document35 pagesObat Lambung (Gi & Tukak Lambung)apt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Pengaruh Hubungan Dokter - Apoteker Terhadap Pelayanan KefarmasianDocument3 pagesPengaruh Hubungan Dokter - Apoteker Terhadap Pelayanan Kefarmasianapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Repro Duks IDocument35 pagesRepro Duks Iapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Gagal JantungDocument7 pagesGagal Jantungapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Patofisiologi SelDocument77 pagesPatofisiologi Selapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Obat HormonalDocument22 pagesObat Hormonalapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLP79% (19)
- Obat PsikiatrikDocument21 pagesObat Psikiatrikapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- AntikankerDocument18 pagesAntikankerapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- AntikoagulanDocument16 pagesAntikoagulanapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLP100% (7)
- EndokrinDocument37 pagesEndokrinapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- HiperlipidemiaDocument35 pagesHiperlipidemiaapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- VitaminDocument33 pagesVitaminapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- TBCDocument30 pagesTBCapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- AstmaDocument20 pagesAstmaapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Laporan Farmakologi Anestesi UmumDocument14 pagesLaporan Farmakologi Anestesi Umumapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLP86% (7)
- AntihipertensiDocument23 pagesAntihipertensiapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Lecture 7 Downstream ProcessDocument40 pagesLecture 7 Downstream Processapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLP83% (6)
- Diabetes MelitusDocument34 pagesDiabetes Melitusapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLP100% (1)
- Lecture 6 Met Primer & SekunderDocument27 pagesLecture 6 Met Primer & Sekunderapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Sediaan SemisolidDocument31 pagesSediaan Semisolidapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLP75% (4)
- Lecture 5 Teknologi PSTDocument26 pagesLecture 5 Teknologi PSTapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- FarmakognosiDocument22 pagesFarmakognosiapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Lecture 4 Teknologi EnzimDocument48 pagesLecture 4 Teknologi Enzimapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet
- Biosintesis Asam AminoDocument29 pagesBiosintesis Asam Aminoapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLP89% (9)
- Pendahuluan SSODocument22 pagesPendahuluan SSOapt. Abdul Rakan Jamaludin, S.Farm., C.Ht, CI, C.N.NLPNo ratings yet