Professional Documents
Culture Documents
Azas Teknik Kimia Pemicu 4
Uploaded by
Tika RisyadCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Azas Teknik Kimia Pemicu 4
Uploaded by
Tika RisyadCopyright:
Available Formats
Azas Teknik Kimia
tentang :
Neraca Energi Sistem Tak Bereaksi
oleh :
KELOMPOK 1
Fransiscus Raymond (110405047)
Atikah Risyad (110405048)
Rahayu Wulandari (110405052
Dasa Haryuwibawa (110405057)
Ekelesia Martina N. (110405077)
Departemen Teknik Kimia
Fakultas Teknik
Universitas Sumatera Utara
2012
PENGANTAR NERACA ENERGI
DEFENISI BEBERAPA ISTILAH
- Sistem adalah bagian dari alam semesta yang dicakup dalam batas-batas lingkup perhatian
analisis. Ruang yang membatasinnya disebut control volume.
- Lingkungan (Environment=surrounding) adalah Bagian dari alam semsta yang berada di
luar batas-batas sistem.
- Sistem terbuka adalah suatu sistem dimana terdapat aliran/pertukaran massa dengan
lingkungan.
- Sistem tertutup adalah suatu sistem di mana tidak terdapat aliran/ pertukaran massa dengan
lingkungan.
- Sifat makroskopik adalah untuk dapat menggambarkan suatu sistem secara kuantitatif.
Perlu diketahui sifat-sifat sistem yang dapat diukur dan hubungan yang ada di antara sifat-
sifat tersebut.
Sifat-sifat sistem yang relevan dengan analisis neraca energi adalah:
- Sifat-sifat makroskopik adalah sifat-sfiat yang menyatakan karakteristik materi secara
bulk dengan memandang materi tersebut sebagai suatu continuum
tf tb
tp
unggun butiran katalis unggun dipandang
dalam medium fluida secara bulk sebagai
suatu continuum
tak dipandang sebagai
suatu continuum
tf = temperatur fluida
tp = temperatur partikel
tb = temperatur bulk
Contoh sifat makroskopik : T, , , Cp, P
- Sifat ekstensifadalah sifat makroskopik yang harganya berbanding lurus dengan
kuantitas zat di dalam sistem.
Contoh V, m dan kandungan Energi
- Sifat intensif: sifat makroskopik yang harganya tidak tergantung dari kuantitas zat di
di dalam sistem.
Contoh: T, P , , fraksi mol, volum spesifik (1/)
Keadaan (State)
Keadaan suatu sistem sepenuhnya terdefenisi bila semua sifat makroskopik sistem
mempunyai harga tertentu.
1. Keadaan tunak atau stasioner (steady state)
Bila di setiap titik di dalam sistem, harga sifat-sifat makroskopik sistem mempunyai
tidak berubah terhadap waktu (harga sifat-sifat tersebut tidak perlu sama dari satu titik
ke titik lain).
2. Keadaan tak tunak atau dinamik (unsteady state)
Bila harga sifat-sifat makroskopik di dalam sistem di steiap titik berubah terhadap
waktu
Keadaan tunak menurut neraca energi adalah bila T dan P di setiap titik di dalam sistem tidak
berubah terhadap waktu
Proses adalah suatu urutan/alur perubahan yang dialami sistem dari keadaan awal ke keadaan
akhir.
Proses isobar: bila urutan kejadiannya berlangsung pada P konstan
Proses isothermal: bila urutan kejadiannya berlangsung pada T konstan
Proses isochoric: bila urutan kejadiannya berlangsung pada V konstan
Fungsi-fungsi keadaan (State functions):
Suatu fungsi yang harganya semata-mata ditentukan oleh keadaan sistem dan tidak
tergantung pada proses (alur kejadian) bagaimana keadaan tersebut dicapai.
Contoh: untuk gas ideal, P = nRT/V adalah suatu fungsi keadaan.
Bila T = T1 dan V = V1, maka P1 = nRT1/V1
Bila T dan V diubah menjadi T2 dan V2, maka P2 = nRT2V2; harga tersebut tidak
bergantung pada proses yang membawa perubahan T1 T2 dan P1P2
Kesetimbangan (Equilibrium)
Suatu sistem berada dalam kesetimbangan (keadaan setimbang), bila keadaan sistem tersebut
tidak berubah terhadap waktu dan akan selalu kembali ke keadaan itu bila terhadap sistem
dilakukan gangguan dalam skala kecil.
Perumusan neraca energi
Karena energi tidak dapat diciptakan dan dimusnahkan, maka dalam suatu sistem, dalam
kurun waktu tertentu:
energi yang masuk ke lingkungan sama dengan energi yang keluar dari sistem ke lingkungan
ditambah akumulasi energi di dalam sistem.
Untuk energi yang masuk ke sistem dan keluar dari sistem, perlu diketahui
- Bentuk energi yang masuk dan keluar
- Mekanisme bagaimana energi yang masuk dan keluar
Untuk akumulasi energi dalam sistem, perlu diketahui:
- Bentuk energi yang berada dalam sistem
- Bagaimana suatu bentuk energi berubah ke bentuk lain
BENTUK BENTUK ENERGI YANG TERKAIT DENGAN MASSA
- Energi potensial (Ep)
Suatu bentuk energi yang tersimpan dalam suatu objek (benda bermassa) berkaitan dengan
tempat kedudukannya terhadap suatu kedudukan rujukan bila benda tersebut berada dalam
medan gravitasi bumi.
Rumus:
Ep = m.g.z
- Energi kinetic (Ek)
Suatu bentuk energi yang dimiliki oleh suatu sistem/objek (benda bermassa) yang bergerak,
diukur relative terhadap kandungan energinya bila dalam keadaan diam pada kecepatan (v)
konstan.
Ek = mv2
- Energi medan magnet dan listrik
Suatu bentuk energi yang terkandung dalam suatu sistem/ objek bila berada dalam suatu
medan magnet ((Ep)m) dan medan listrik ((Ep)e).
- Energi dalam (U)
Suatu bentuk energi yang terkandung dalam suatu sistem yang terkait dengan energi atom
dan molekul yang menyusun benda itu.
U merupakan fungsi keadaan yang harganya terdefinisi secara pasti oleh keadaan sistem
Akumulasi energi di dalam sistem = Ep + Ek + (Ep)m + (Ep)e + U
BENTUK BENTUK ENERGI DALAM TRANSISI
Pertukaran energi antara sistem dengan lingkungannya dapat terjadi dalam 4 cara yaitu
melalui:
1. perpindahan massa.
2. kerja yang dilakukan
3. perpindahan panas
4. pengaruh medan
Karena energi terkandung di dalam benda (bermassa), maka bila terjadi perpindahan massa
selalu akan terjadi perpindahan energi (karena terbawa oleh massa itu)
- Kerja (W)
Kerja merupakan hasil kali gaya dengan jarak litasan benda yang dikenakan pada gaya
tersebut
W = F. Z atau bila F konstan
}
=
2
1
z
z
dZ F W
Bila suatu sistem melakukan kerja ke lingkungan , maka W bertanda (+)
Sebagian energi sistem berpindah ke lingkungan dan sebaliknya.
Beberapa bentuk kerja: kerja poros (Shaft work), kerja listrik, kerja ekspansi kompresi
Kerja ekspansi kompresi contohnya piston
F = P.A
Maka Ws = P.A dZ di mana dZ = dV/A atau dV = A dZ
Ws = dV
Bila P konstan : Ws = P. V = P(V2 - V1)
Bila P bervariasi :
}
=
2
1
V
V
dZ P W
Energi yang diterima lingkungan We Ws (karena ada kehilangan)
Untuk memperhitungkan kehilangan digunakan koefisien efisiensi ()
Bila kerja dilakukan oleh sistem ke lingkungan:
We = s Ws
Bila kerja dilakukan oleh lingkungan ke sistem:
Ws = e We
Di mana Ws, We adalah kerja yang diterima dan e, s < 1,0
- Panas
Bila sistem beruhu Ts ditempatkan di lingkungan bersuhu Te di mana Te > Ts, maka Ts
akan meningkat dan Te akan menurun, demikian sebaliknya.
Terjadi perpindahan energi melalui mekanisme konduksi atau konveksi. Bentuk energi
yang dipindahkan karena perbedaan suhu / panas
Bila sistem menerima panas dari lingkungan diberi tanda (+)
- Radiasi elektromagnetik
Rambatan gelombang elektromagnetik yang mengenai sistem dapat menyebabkan
berpindahnya energi. Mekanisme perpindahan energi ini disebut radiasi. Bentuk radiasi
yang penting adalah yang melibatkan gelombang elektromagentik pada interval infra
merah.
Raidasi terjadi pada suhu tinggi.
Energi dapat berpindah dari sistem ke lingkungan melalui berbagai mekanisme dan dalam
berbagai bentuk
Rangkuman bentuk energi :
Penyebab Mekanisme Bentuk
Aliran/gerak bahan dan
perpindahan massa
konveksi Ep, Ek dan U
Perbedaan suhu Konduksi dan konveksi Panas
Gerak mekanis (poros
atau ekspansi-kompresi)
mekanik Kerja
Radiasi elektromagetik
mengenai sistem atau
memancar dari sistem
radiasi Panas
NERACA ENERGI SISTEM TAK BEREAKSI
Untuk menggunakan persamaan neraca energi sistem terbuka dan tertutup dikembangkan
pada bab sebelumnya, yang mana perlu harga dari entalpi dan fungsi energi dalam yang
terlihat pada persamaan ini Q = H2 H1, kita harus mampu mengevaluasi H pada akhir dan
awal kedudukan.
KARAKTERISTIK KEADAAN SISTEM
Kaidah Fasa
secara umum, sifat intensif utama yang digunakan untuk mengkarakterisasi keadaan
setimbang dari sistem adalah temperatur, tekanan, dan komposisi dari masing-masing fase.
Namun, tidak semua sifat ini perlu ditetapkan untuk menentukan keadaan setimbang dari
sistem. sebaliknya, ada sejumlah yang tepat dari sifat sistem yang bila ditentukan, otomatis
mendefinisikan negara equiibrium dan dengan demikian perbaikan nilai dari sifat intensif
tersisa. Jumlah sifat tersebut yang disebut derajat kebebasan termodinamika sistem, dan itu
tergantung pada jumlah komponen kimia dan jumlah fase hadir dalam sistem. Hubungak n
yang tepat antara derajat kebebasan D, jumlah komponen C, dan jumlah fase yang disebut
kaidah fase dan diberikan hubungan
D = C + 2
Dimana D = jumlah derajat kebebasan sistem
C = jumlah komponen kimia bila tidak ada reaksi kimia
= jumlah fasa yang ada pada kesetimbangan
Untuk sistem tak bereaksi, sebuah komponen kimia sebagaimana digunakan dalam
konteks kaidah fasa adalah sama seperti jenis molekul. Dengan demikian, pada kasus tak
bereaksi, C = S, dimana S adalah jumlah spesies yang digunakan pada konteks neraca massa.
Pada kasus yang bereaksi , jumlah komponen adalah sama dengan jumlah spesies dikurang
jumlah reaksi kimia bebasnya, p(), terjadi antara spesies ini, sehingga
C = S p()
Jika komponen C ditunjukkan pada pengukuran normal seperti massa atau fraksi mol,
sebagaimana pada neraca massa, hanya C 1 pada komposisi ini diketahui tak bebas.
Sistem Satu Komponen
Untuk satu komponen sistem tak bereaksi, kaidah fasa diturunkan menjadi
D = 3
Selama derajat kebebasan tidak menjadi negatif, kaidah fasa mengindikasikan bahwa
komponen murni dapat eksis di hampir 3 fasa pada kesetimbangan.
Sistem 1 komponen 2 fasa
Misal : air murni dalam keadaan uap (steam ) yang setimbang dengan cairannya ( buble
point)
Karena = 2, maka D = 3 2 = 1
D = 1 artinya
- Salah satu dari T; P atau boleh ditetapkan, tetapi tidak boleh sekaligus
- Bila salah satu dari T atau P atau ditetapkan nilainya, maka variabel lainnya sudah
tertentu nilainya.
- Variabel lain yang nilainya belum diketahui tersebut, daapat ditentukan dari :
o Tabel atau kurva tekanan uap murni
o Persamaan empiris untuk tekanan uap :
- Persamaan antoine
- Persamaan tekanan uap Riedel
o Untuk steam (uap air murni) : dari tabel steam
Tekanan uap adalah tekanan dimana uap dan cairan dari suatu komponen murni
berada dalam kesetimbangan. Kurva tekanan uap murni dalam bentuk persamaan empiris,
antara lain : Persamaan Antoine,
Persamaan Antoine :
Dimana p = tekanan uap murni
T = suhu pada saat setimbang
A, B, C = konstanta konstanta untuk tiap komponen
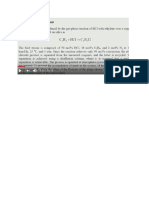
Contoh 7.1 tekana uap aseton diberikan oleh
Dimana p dalam mmHg dan T dalam K. Sebuah campuran uap cair dari aseton diperoleh
setimbang pada 100 mmHg. T kesetimbangan ?
Sehingga, T = 245.40 + 34.5228 = 279.22
Pada kasus sistem fase gas atau cair , hubungan antara keseimbangan temperatur,
tekanan , dan volume molar dituliskan pada persamaan keadaan . persamaan keadaan paling
sederhana adalah gas ideal, yaitu :
PV = RT
Dimana R adalah konstanta gas = 8, 3143 J / mol. K
Persamaan keadaan kompleks lain misalnya persamaan Redlich Kwong
P
T1/2 V (V + b))-1
Dimana a dan b adalah konstanta empiris suatu komponen.
Multi komponen, sistem multi fase
Sebagaimana jumlah komponen dan meningkatnya fase, spesifikasi dan penentuan
keseimbangan kedudukam menjadi peningkatan yang kompleks. Umumnya, tambahan
spesifikasi T, P, atau , juga diperlukan untuk menspesifikasi komposisi fasa. Sebagai
contoh, untuk dua komponen campuran gas, aturan fasa mengindikasi suatu derajat
kebebasan yaitu 3
D = 2 -1 + 2 = 3
Sehingga, jika temperatur dan tekanan terspesifikasi dan campuran dua gas diasumsikan
mengikuti gas ideal, kemudian campuran volume molar dapat dihitung dengan
Untuk campuran cair gas, hubungan antara fraksi mol komponen pada dua fase ditentukan
oleh faktor K.
Ki =
Dimana yi adalah fraksi mol spesies i pada fase uap dan xi adalah fraksi mol fasa cair. Untuk
beberapa campuran sederhana , fungsi Ki pada T dan P
Ki = Ki (T,P)
Untuk campuran komponen dengan stuktur molekul yang sama Ki dapat dihitung dengan
membandingkan tekanan uap pada spesies i yang diberikan pada temperatur tekanan total
Ki =
yang diebut hukum Roult
K1 =
K2 =
K1 =
K2x2 = y2
X1 + x2 = 1
Kita memperoleh substitusi definisi faktor K pada persamaan
= 1
Ki = Ki (T, P, X1, X2)
Bubble Point dan Dew Point
Bubble Point adalah temperatur dimana gelembung gelembung uap terbentuk pertama kali
ketika campuran fasa air dipanaskan perlahan lahan
Bubble-point temperature problem -- P,x given -- T,y unknown.
y
P x
P
i
i
sat
i
= = 1
Dew-point pressure problem -- T,y given -- P,x unknown
( )
x
Py
P
x
P
y P
i
i
i
sat
i
i i
sat
= =
=
1
1
/
Dew-point temperature problem -- P,y given -- T,x unknown.
x
Py
P
i
i
i
sat
= = 1
Dari rumus
Diperoleh :
( )
0
) 1 ( 1
1
) , (
=
+
= = =
i
i i
sat
i
i
i
i
K V
K z
T P f
P
P
x
y
K
NERACA ENERGI MENGGUNAKAN DATA TERMODINAMIKA TABULAR
Dalam sistem komponen tunggal, tidak lebih dari dua atau bahkan tidak ada variabel yang
harus ditentukan, tergantung pada jumlah fase hadir dalam sistem. Akibatnya, untuk
komponen tunggal, entalpi spesifik dan fungsi spesifik energi dalam dapat dinyatakan sebagai
dua fungsi terbanyak dari salah satu tiga variabel P, T, dan V. Oleh konvensi, fungsi entalpi
spesifik untuk komponen tunggal murni dinyatakan dalam T dan P, sedangkan fungsi
komponen energi dalam murni spesifik dinyatakan dalam T dan V. Jadi, dapat dituliskan :
= (T . P) dan = (T . )
Tentu saja, di daerah T dan P dimana komponen murni ada sebagai fase tunggal, baik
T dan P akan perlu ditetapkan untuk menentukan entalpi tersebut. Namun, di daerah di mana
dua tahap akan ada dalam kesetimbangan, T dan P tidak dapat ditentukan, dan karenanya
fungsi entalpi spesifik tidak bisa secara efektif menjadi fungsi dari satu variabel. Untuk
keperluan perhitungan keseimbangan energi, komponen fungsi murni entalpi spesifik harus
tersedia sebagai fungsi aljabar eksplisit T dan P dalam kasus fase tunggal dan T dalam kasus
fase ganda sehingga bahwa bisa dievaluasi secara langsung. Diperlukan fungsi entalpi untuk
masing-masing fase tunggal seperti padat, cair, dan uap, serta untuk fase ganda. Fungsi
tersebut tersedia untuk beberapa zat seperti air, amonia, udara, dan refrigeran standar.
Namun, mereka biasanya cukup rumit, mengandung banyak istilah, dan cukup sulit untuk
mengevaluasi perhitungan manual. Sebagai contoh, entalpi fungsi spesifik untuk uap air atau
uap adalah fungsi aljabar yang melibatkan sekitar 60 konstanta ditentukan oleh data
eksperimen. Selain itu, untuk menggunakan fungsi tersebut, perlu diketahui dulu fase yang
ada. Oleh karena itu, diperlukan hubungan tambahan seperti persamaan tekanan uap serta
persamaan keadaan yang akan memungkinkan untuk dilaksanakannya interkonversi P, T, V.
Oleh karena itu, untuk perhitungan manual, entalpi komponen murni spesifik dan fungsi
energi dalam ditulis dalam bentuk tabel. Representasi tabular dapat dibuat karena fungsi
keadaan akan melibatkan paling banyak dua variabel bebas yang dapat diatur dalam baris dan
kolom. Representasi tabular juga memungkinkan penyisipan informasi yang mengidentifikasi
batas fase transisi dan yang memungkinkan interkonversi variabel keadaan melalui
persamaan data. Tabel yang dihasilkan berisi semua informasi yang diperlukan untuk
termodinamika spesies komponen murni dan karenanya disebut tabel termodinamika.
TABEL ENERGI
Tabel energi yang terdapat di Appendiks 8 terdiri dari tiga bagian : tabel temperatur
uap jenuh, tabel tekanan uap jenuh, dan tabel uap super-panas. Ketiga tabel tersebut
menampilkan nilai volume spesifik, yang merupakan kebalikan dari kepadatan, energi dalam
spesifik, dan entalpi spesifik. Tabel uap jenuh menampilkan sifat cair air dan uap saat berada
pada kondisi jenuh yaitu dalam kesetimbangan satu sama lain. Jika sistem komponen murni
berfasa ganda, derajat kebebasannya adalah 1, maka tabel uap jenuh memberikan nilai
volume spesifik, entalpi, dan energi dalam sebagai fungsi dari satu variabel bebas. Tabel
pertama menggunakan temperatur sebagai variabel bebas, tabel kedua menggunakan tekanan
sebagai variabel bebas. Perhatikan pada tabel uap jenuh, di samping daftar entalpi air dan
uap, juga ada kolom ketiga berjudul "penguapan". Kolom ini merupakan perbedaan antara
entalpi uap spesifik dan air cair dan disebut entalpi penguapan, atau panas laten. Terakhir,
perhatikan bahwa pada 0,01oC dan 0,00611 bar (105 Pa), energi dalam cairan air jenuhnya
adalah nol. Ini adalah keadaan referensi untuk tabel uap ini, dan nilai nol untuk energi dalam
spesifik dalam nilai referensi yang diberikan.
Tabel uap super-panas menampilkan entalpi spesifik , energi dalam spesifik dan
volume spesifik uap sebagai fungsi tekanan dan temperatur. Karena derajat kebebasan
termodinamika komponen tunggal sistem fasa tunggal adalah 2, kedua variabel harus
terspesifikasi untuk menetapkan nilai dari variabel lain, , dan nilai fungsi dan . Tabel ini
juga menampilkan temperatur jenuh di bawah tekanan dan termasuk uap jenuh dan sifat air di
kolom kedua dan ketiga. Terakhir, tabel ini juga memperlihatkan tekanan kritis 221.2 bar dan
temperatur kritis 374.15 oC, dimana tidak ada lagi perbedaan antara uap dan sifat air encer.
Contoh 7.6 :
(a) Tentukan nilai entalpi dari 1 kg cairan air jenuh pada 80 oC dan tentukan tekanan
uap jenuhnya!
Penyelesaian :
(a) Untuk menentukan kejenuhan pada temperatur yang diberikan, gunakan tabel
temperatur uap jenuh. Pada 80 oC, tekanan uap jenuhnya adalah 0.4736 bar dan
entalpi spesifiknya adalah 334.9 kJ/kg. Maka entalpi dari 1 kg menjadi 334.9 kJ.
Interpolasi
Misalnya, pada tabel tekanan, data yang diberikan yaitu pada 100 dan 105 bar, tetapi
yang dibutuhkan adalah entalpi spesifik uap pada 103.0 bar. Jadi, entalpi yang dibutuhkan
berada antara 2727.7 dan 2718.7 kJ/kg. Sebuah pendekatan yang memadai dalam perhitungan
teknik adalah dengan menggunakan interpolasi linear antara nilai tabular yang berdekatan.
Masalah umum interpolasi adalah bahwa diberikan nilai fungsi y(x) pada xU dan pada
xL, dinotasikan dengan yU dan yL, berturut-turut, ditaksir nilai dari y(x) berada pada titik
tengah xi. Bentuk interpolasi sederhana :
atau
Persamaan ini dikenal sebagai persamaan linear untuk yi dalam bentuk xi. Perhatikan
bahwa beberapa data diinterpolasikan untuk variabel bebas x yang sama., kemudian
persamaan di atas diterapkan untuk tiap-tiap data yang terpisah.
Contoh 7.7 :
Tentukan entalpi spesifik dan volume untuk uap pada 5 bar dan 320 oC.
Penyelesaian :
Pada 5 bar, dari tabel tekanan, temperatur jenuh yaitu 151.8 oC. Uapnya uap panas.
Tabel uap panas memiliki data untuk 300 dan 350 oC. Untuk menaksir harga dan pada
320 oC, lakukan interpolasi. Interpolasikan volume spesifik :
= 0.542 m3/kg
Interpolasi untuk entalpi,
= 3106.2 kJ/kg
Bobot Uap
Perhitungan uap sering dibutuhkan untuk menangani campuran uap dan cairan air.
Misalnya, uap digunakan sebagai media pemanasan dan mengembun sebagian. Hasil
campuran terdiri dari uap jenuh dan tetesan cairan air jenuh. Fraksi massa uap air dalam
campuran cairan dan uap, ditunjukkan oleh X, yang dikenal dengan bobot uap. Menurut
defenisi, saat X = 1, uap adalah semua uap air jenuh; saat X = 0, uap adalah semua cairan
jenuh. Uap dengan kualitas menengah untuk kedua ekstrim dikatakan sebagai uap basah.
Karena uap basah terdiri dari fasa jenuh, maka tabel uap jenuh dapat digunakan
untuk menghitung entalpi spesifik, energi dalam, dan volume campuran cairan-uap air. Jika
bobot uap diketahui, maka sifat campuran dapat dihitung sebagai kombinasi linear dari sifat
fasa jenuh tersendiri. Sehingga,
Sebaliknya, jika salah satu sifat campuran diketahui, bobot dapat dihitung dari
hubungan persamaan di atas dengan penyelesaian sederhana untuk X.
Contoh 7.8 :
Tentukan tekanan, volume spesifik, entalpi, dan energi dalam dari uap basah pada 230
oC dengan bobot 0.4 .
Penyelesaian :
Jika uap memiliki bobot antara 0 dan 1, maka kedua fasa harus diketahui, dan ini bisa
diasumsikan bahwa fasa ini berada pada titik kesetimbangan. Jadi, dari aturan fasa, satu sifat
makroskopik cukuplah untuk menetnukan keadaan sistem. Dari tabel tekanan uap jenuh,
diketahui bahwa pada 230 oC tekanan jenuhnya adalah 28 bar. Sifat fasa jenuh yaitu :
Air Uap Air Uap Air Uap
0.001209 0.0714 987.1 2602.1 990.5 2802.0
Gunakan hubungan persamaan campuran, sehingga :
APLIKASI NERACA ENERGI : SISTEM TERTUTUP
Jika diketahui sebuah tabulasi luas dari sifat termodinamika seperti untuk uap,
masalah keseimbangan energi larutan dalam sistem tertutup umumnya cukup mudah. Seperti
pada bab 6.5.3, keseimbangan energi tereduksi menjadi bentuk :
(
Seringkali, istilah energi kinetik dan energi potensial dianggap nol atau diabaikan,
yang mengarah ke penyederhanaan :
(
)
Namun, kebanyakan pada aplikasi sistem tertutup dalam kepentingan teknik kimia,
istilah kerja akan timbul karena ekspansi atau kompresi. Oleh karena itu, keseimbangan
tereduksi lebih lanjut lagi :
(
)
Terakhir, jika tekanannya konstan, maka dan bentuk entalpi
(
) dapat digunakan.
Dari bentuk sederhana persamaan, upaya dalam penyelesaian masalah neraca energi
sistem tertutup direduksi untuk penentuan nilai yang sesuai untuk fungsi dan untuk
dimasukkan ke dalam persamaan neraca.
Contoh 7.10 :
Satu kilogram uap pada tekanan 1 bar, terkandung dalam silinder dengan luas
penampang 1.69 m2, bebas bergerak, penutup rapat, berat tetap, seperti yang terlihat pada
gambar 7.3. silinder dipanaskan dari luar untuk mencapai temperatur uap dari 100 oC hingga
300 oC. Asumsikan tidak ada panas yang hilang ke lingkungan, hitung jumlah kalor yang
dibutuhkan untuk proses ini.
Penyelesaian :
Mengenai sistem, terdiri dari uap yang terkandung dalam silinder. Dengan tidak
adanya uap yang bocor selama proses berlangsung, sistem benar-benar tertutup. Gas yang
mengembang karena pemanasan akan mendorong penutup silinder ke atas dan tekanan
konstan tetap dipertahankan. Oleh karena itu, bentuk persamaan entalpi neraca energi sistem
tertutup dapat digunakan. Yaitu,
H + PE + KE = Q
Karena sistem tak bergerak, energi kinetiknya nol. Namun akan ada perubahan dalam
elevasi dari pusat massa sistem disebabkan oleh gas yang mengembang. Perubahan itu
kemungkinan kecil sekali, meskipun begitu, kita harus tetap menguasai energi potensial
dalam persamaan keseimbangan.
Dari tabel uap superpanas, pada 100 oC dan 1 bar, entalpi uap spesifiknya 2676 kJ/kg
dan volume spesifiknya 1,69 m3/kg; sementara pada 300 oC dan 1 bar, entalpi dan volume
spesifiknya yaitu 3074 kJ/kg dan 2,64 m3/kg. Dengan menerapkan persamaan neraca di atas,
kita hitung bahwa :
Jika ketinggian pusat massa silinder diketahui sebagai z = L/2 =
, maka,
(
Berat penutup
L2 P1 A = 1,69 x 105 N
L1 = 1 m
Q
Gambar 7.3 Contoh Silinder Uap
Jelas, istilah energi potensial cukup signifikan, seperti biasanya dalam kasus-kasus
yang melibatkan pemanasan dan pendinginan.
Selama proses berlangsung, sistem tidak melakukan kerja ekspansi. Kerja itu dapat
dihitung menggunakan persamaan :
dimana, jika P konstan, tereduksi menjadi :
Jadi, dari jumlah total energi yang ditransfer ke sistem sebagai panas (398 kJ), kira-
kira seperempatnya (95 kJ) digunakan oleh sistem dalam kerja ekspansi. Akibatnya, energi
dalam sistem meningkat hanya dengan selisih , sehingga :
Perhitungan ini dapat dicek langsung menggunakan nilai U yang diketahui pada tabel.
Nilai Energi Relatif dan Mutlak
Nilai
dan
yang terdapat dalam persamaan neraca energi sebenarnya nilai entalpi
dan energi dalam mutlak. Namun, nilai entalpi dan energi dalam yang terdapat pada tabel uap
hanyalah nilai relatif. Dengan kata lain, mereka merupakan nilai-nilai relatif untuk
T1 = 100
o
C
P1 = 1 bar
V1 = 1,69 m
3
diasumsikan sebagai nilai referensi titik triple nilai nol dari energi dalam. Hubungan antara
keduanya yaitu pada kasus fungsi energi dalam, diberikan :
dimana
adalah energi dalam mutlak dan
adalah
energi dalam relatif untuk keadaan referensi
.
Kita bisa menggunakan entalpi relatif untuk tujuan neraca karena energi internal dari
keadaan referensi sama sekali terhapus dalam persamaan neraca. Artinya, jika
disubstitusikan ke dalam persamaan hukum pertama, kita dapatkan :
(
) [(
] (
)
Jadi, persamaan neraca dapat dituliskan dalam hal baik energi dalam relatif ataupun
mutlak. Jika energi dalam mutlak tidak diketahui, gunakan energi dalam relatif dan biasanya
menghapus subskrip r.
Seluruh nilai energi dalam atau entalpi yang digunakan dalam perhitungan neraca
disebut keadaan referensi yang sama. Misalnya, jika energi dalam untuk keadaan awal
diperoleh dari satu sumber sementara energi dalam untuk keadaan akhir diperoleh dari
tabulasi yang lain di mana mungkin saja mempunyai rentang P dan T yang tinggi, ini penting
untuk mengecek bahwa kedua sumber menggunakan keadaan referensi nol yang sama.
Koreksi dilakukan sebagai berikut. Diperkirakan satu tabel menjabarkan energi dalam relatif
untuk keadaan referensi a, sementara tabel lain memberikan energi dalam untuk zat relatif
yang sama untuk keadaan referensi b. Untuk mengubah entalpi relatif terhadap a, (U Ua),
ke entalpi relatif terhadap b, (U - Ub), secara sederhana :
(U - Ub) = (U Ua) (Ub Ua)
Dengan kata lain, entalpi relatif dikoreksi terhadap a dengan mengurangkan entalpi
relatif keadaan referensi b terhadap keadaan referensi a. Koreksi perhitungan entalpi referensi
diilustrasikan pada contoh berikut.
Contoh 7.12 :
Hitung panas yang dibutuhkan untuk mencapai temperatur dari 1 kg uap pada 885 bar
dari 500 oC sampai 816 oC, diketahui entalpi spesifik pada temperatur akhir adalah 1130
kJ/kg relatif terhadap uap jenuh pada 1,01325 bar (1 atm).
Penyelesaian :
Jelas, pada tekanan konstan, Q = 1 kg. Entalpi pada kondisi awal, dengan
menginterpolasi dari tabel uap super-panas, yaitu
Entalpi ini relatif untuk cairan air pada titik triple. Untuk mengubah entalpi relatif yang
diketahui dari 1130 kJ/kg pada keadaan akhir untuk sebuah entalpi relatif terhadap titik triple,
digunakan rumus koreksi,
(
) (
) [
]
Jumlah [
] hanyalah entalpi dari uap pada 1 atm relatif terhadap titik
triple. Dari tabel tekanan uap jenuh, jumlahnya adalah 2676,0 kJ/kg. Jadi,
(
Terakhir, Q = m(
= 1 kg(3806 2409,6) kJ/kg = 1196,4 kJ
Penggunaan dari entalpi relatif yang tak terkoreksi tentu saja telah menyebabkan cukup
kesalahan pada perhitungan Q. Dalam contoh ini, hal itu akan menyebabkan negatif pada Q.
APLIKASI NERACA ENERGI : SISTEM TERBUKA
Sebagai hasil di sesi 6.5, bentuk umum dari persamaan neraca energi untuk sistem
terbuka melibatkan beberapa aliran masuk dan keluar adalah,
Bentuk energi dalam dari persamaan sistem terbuka tidak umum digunakan karena
membutuhkan evaluasi terpisah dari P. Hal utama dalam penerapan persamaan ini terhadap
masalah spesifik yaitu :
1. Jelas mendefenisikan batas sistem
2. Hati-hati mempertimbangkan hal yang dapat diabaikan dalam pemecahan masalah
3. Memeriksa semua kontribusi panas dan kerja yang terlibat
4. Memeriksa semua sumber data entalpi untuk komponen yang diketahui menggunakan
keadaan referensi.
Kita ilustrasikan hal ini dengan contoh soal yang menggunakan data entalpi tabel uap.
Contoh 7.13 :
Uap pada 200 oC dan 7 bar memasuki sebuah pipa horizontal dengan kecepatan tetap
pada 60 m/s. Uap keluar pada kecepatan 600 m/s dan tekanan menurun 1,4 bar. Hitung
temperatur dan banyak uap yang keluar.
Penyelesaian :
Sebuah pipa adalah sebuah alat yang berfungsi untuk meningkatkan energi kinetik
dari fluida dengan menurunkan tekanan. Prosesnya biasanya diasumsikan untuk cara
adiabatik karena kerugian atau keuntungan melewati dinding pipa biasanya dapat diabaikan
untuk istilah energi yang lain.
Sistem yang sedang dipertimbangkan, terlihat pada gambar 7.4, yaitu sebuah sistem
terbuka jika uap terus menerus memasuki dan meninggalkan batas sistem. Selain itu, sistem
jelas mempunyai masukan dan keluaran tunggal. Karena itu, persamaan neraca energi yang
berlaku yaitu,
Dengan asumsi, sistem mengalami proses adiabatik; jadi, dQ/dt = 0. Juga, jika
dinding pipa kaku, tidak ada kerja ekspansi atau pemampatan yang dilakukan oleh sistem;
oleh karena itu, dW/dt = 0. Selanjutnya, jika aliran masuk dan keluar berada pada tingkat
yang sama, tidak ada perubahan dalam ketinggian, z1 = z2. Terakhir, dari sebuah neraca
massa sederhana, F2 = F1 = F. Persamaan neraca energi tereduksi menjadi,
(
) (
)
Membagi oleh aliran massa dan penyelesaian untuk
, diperoleh :
Pada 200 oC dan 7 bar, uapnya super-panas dan telah diinterpolasi entalpi spesifik
dari 2843,8 kJ/kg. Jika dua kecepatan diketahui, kita bisa menghitung
Untuk menentukan temperatur uap keluar, diketahui bahwa tekanannya 1,4 bar, cek
tabel uap jenuh untuk menentukan apakah entalpi yang dihitung melampaui entalpi uap
jenuh. Entalpi uap jenuh pada 1,4 bar adalah 2690,3 kJ/kg; jadi, uap yang keluar pasti basah
dan temperaturnya pasti setara terhadap temperatur jenuh pada 1,4 bar, yaitu, 109,3 oC.
Jumlahnya dapat dihitung dengan mudah dari :
2665,6 = 2690,3 X + 458,4(1 X)
Penyelesaiannya adalah X = 0,989, dengan kata lain, 0,011 dari uap terkondensasi.
Catatan bahwa bahkan dengan kecepatan keluaran yang sangat tinggi 600 m/s, energi
kinetiknya hanya sekitar 6 % dari entalpi masukan. Biasanya, dalam aplikasi proses kimia,
kecepatan alirannya kurang dari 50 m/s, di mana energi kinetiknya akan brjumlah 2,5 kJ/kg,
atau kurang dari 0,1 % dari entalpi.
NERACA ENERGI TANPA TABEL TERMODINAMIKA LENGKAP
Cara Menggunakan Tabel Uap (Steam Table)
Contoh :
1. Air pada tekanan 1 bar dan temperatur 99,6 C berada pada keadaan jenuh (keadaan jenuh
artinya uap dan cairan berada dalam keadaan kesetimbangan atau berada bersama-sama pada
system yang sama), maka dari steam table didapatkan :
Hcairan(99,6 C; 1 bar) = 417,5 kJ/kg
Huap(99,6 C; 1 bar) = 2675,4 kJ/kg
2. Air pada temperatur 200 C dan tekanan 10 bar berada dalam keadaan fasa uap superheated
dengan H = 2828,3 kJ/kg
3. Entalpi (H) untuk air pada tekanan 1 bar dan temperatur 127 C tidak tercantumkan di dalam
tabel, maka dicari nilainya dengan cara interpolasi.
H (100 C; 1 bar) = 2676 kJ/kg
H (150 C; 1 bar) = 2780 kJ/kg
H (127 C; 1 bar) = ? kJ/kg
Tugas :
Kondisi
P, bar T, C (fasa),cair/c
air-uap/uap
H, kJ/kg
a 150 50 ? ?
b 150 300 ? ?
c 0,1 50 ? ?
d 0,1 300 ? ?
e 1 99,6 ? ?
f 1 99,6 ? ?
Penggunaan Neraca Massa-Energi : Sistem Terbuka
Sistem dibagi menjadi 3 :
a. Sistem terbuka jika system tersebut menerima masukan massa dan energi atau melepaskan
massa dan energi keluar system.
b. Sistem tertutup jika system tersebut tidak mengalami pemasukan massa atau pengeluaran
massa. Sebuah system mengalami pemasukan ataupun pengeluaran energi, yang dapat berupa
panas, kerja atau listrik atau magnet
c. Sistem terisolir jika system tersebut tidak megalami pemasukan dan pengeluaran massa
dan energi dalam bentuk apapun
Secara umum persamaan neraca energi untuk system terbuka adalah :
Q W = Fk(H + gz + v2)k - Fm(H + gz + v2)m
(persamaan di atas dapat dilihat pada buku Reklaitis hal. 424)
Q Panas yang masuk atau keluar system melalui dinidng system akibat perbedaan
temperatur system dengan lingkungan
( + ) bila panas masuk system
( - ) bila panas keluar system
Q = 0 (system adiabatic, artinya jika system tersebut tidak mengalami pemasukan
atau pengeluaran energi dalam bentuk panas)
W Kerja yang berpindah melalui dinding system sebagai akibat :
1. perbedaan tekanan system dan lingkungan, yang diwujudkan dengan perubahan volume system
2. perbedaan tekanan lingkunagn dengan system ditempat masukan, dan perbedaan tekanan
system dengan lingkungan ditempat keluaran
3. kerja poros yaitu yang berhubungan dengan lingkungan,
( + ) bila kerja keluar system
( - ) bila kerja masuk system
Dari hasil pengamatan pada contoh kasus 7.14 hal 426 pada buku Reklaitis, besarnya nilai energi
potensial dan energi kinetic relative jauh lebih kecil bila dibbandingkan dengan nilai entalpi (H),
maka dalam hal ini (neraca massa-energi) kita dapat mengabaikannya.
Jadi persamaan neraca energi dapat disederhanakan :
Q W = FkHk - FmHm
Contoh kasus :
Hitunglah kerja (W) yang diberikan ??
Penyelesaian :
Tentukan entalpi spesifik (H) untuk kedua kondisi baik masukan ataupun keluaran
P = 5 bar
T = 50 C H = 209,80 kJ/kg P = 5 bar
= cairan T = 60 C H = 259,67 kJ/kg
P = 5 bar = cairan
T = 100 C H = 419,51 kJ/kg
= cairan interpolasi
Neraca massa total : F1 = F2 = 1,5 kg/s
Q = 0, maka
-W = F2 H2 F1 H1 = 1,5 (259,67 251,74) kJ/s = 11,9 kWatt
W = -11,9 kWatt
Tugas : Berapakah kerja (W) yang diberikan dalam satuan Kwatt??
Contoh kasus 7.15 pada Reklaitis, hal 429 :
Uap air digunakan untuk memanaskan 300 kg/jam air proses dari temperatur 50 C menjadi 150 C
pada tekanan 5 bar, alat penukar panas yang digunakan adalah double pipe. Uap air yang
digunakan adalah uap jenuh tekanan 10 bar.
Penyelesaian :
Q = 0 = FkHk - FmHm
0 = FAP,k x H(150 C, 5 bar) + FU,k x Hw(10 bar) - FAP,m x H(50 C, 5 bar)
- FU,m x Hv(10 bar)
FAP,k = FAP,m = 300 kg/jam ; FU,k = FU,m = F
H(150 C, 5 bar) = 632,2 kJ/kg
H(50 C, 5 bar) = 209,7 kJ/kg
Hw(10 bar) = 762,6 kJ/kg
Hv(10 bar) = 2776,2 kJ/kg
0 = 300 x 632,2 + F x 762,2 300 x 209,7 F x 2776,2
F = 629,5 kg/jam
Tugas : G.V. Reklaitis hal 473 no. 7.24
Tabulasi entalpi dan energi dalam, seperti halnya steam table tidak tersedia untuk kebanyakan
senyawa, yang tersedia datanya adalah data kapasitas panas. Untuk apa data kapasitas panas ?
Cara menggunakan data kapasitas panas
Data kapasitas panas dapat digunakan untuk menghitung perubahan entalpi dari suatu senyawa
yang terlibat dalam suatu proses tertentu dan tidak mengalami perubahan fasa (panas sensibel)
H2(T2,P) H1(T1,P) = Cp (T) dT G.V. Reklaitis, hal 440
Perubahan entalpi dengan tekanan tetapsuatu proses kebanyakan dipertahankan
pada tekanan tetap
Cp(T) artinya kapasitas panas sangat dipengaruhi oleh variable temperatur, tetapi
bukan berarti kapsitas panas tidak dipengaruhi oleh tekanan, akan tetapi pengaruh temperatur
jauh lebih besar daripada tekanan. Oleh karena itu, seringkali pengaruh tekanan terhadap
kapasitas panas diabaikan. (Reklaitis hal 437)
Data kapasitas panas dapat dilihat di G.V. Reklaitis hal 643 (Gas ideal, J/mol.K), hal 657
(kapasitas panas cairan, J/mol.K)
Contoh kasus :
1. Dua aliran air dicampurkan yaitu aliran-1 memiliki temperatur 30 C dan aliran-2 memiliki
temperatur 80 C. Laju alir aliran-1 300 kg/jam dan laju aliran-2 100 kg/jam. Hitunglah temperatur
campuran. Cp,air = 4,2 kJ/(kg. C)
Penyelesaian :
- Selesaikan dahulu persamaan neraca massa :
Neraca massa total : F1 + F2 = F3 = 400 kg/jam
- susunlah persamaan neraca energi :
Q = F3 [H3(T3) H3(Tref)] F1 [H1(T1) H1(Tref)] F2 [H2(T2) H2(Tref)]
Q = 0
Tref = 25 C
Maka,
0 = F3 [H3(T3) H3(25C)] F1 [H1(30C) H1(25C)] F2 [H2(80C) H2(25C)]
H3(T3) H3(25C) = Cpair (T) dT = 4,2 (T3 25)
H1(30C) H1(25C) = Cpair (T) dT = 4,2 (30 25)
H2(80C) H2(25C) = Cpair (T) dT = 4,2 (80 25)
0 = 400(4,2)(T3 25) 300 (4,2)(30-25) 100 (4,2)(80-25)
T3 = 42,5 C
2. Aliran gas alam setelah mengalami kompresi didinginkan dalam heat exchanger dari keadaan
masuk dengan temperatur T1= 38 C menjadi T2 = 20C. Laju alir gas alam adalah 100 mol/detik.
Komposisi (disederhanakan) dan data kapasitas panas gas alam (disederhanakan) disajikan dalam
tabel di bawah ini:
Tentukan panas yang harus dibuang dari system aliran gas alam ini. Pengaruh perubahan tekanan
terhadap entalpi diabaikan :
Komponen Komposisi,fraks
i mol
Cp, J/mol.K
CH4 90 % 38,387
CO2 10% 19,022
Penyelesaian :
- Soal ini memberikan gambaran tentang penggunaan data kapasitas panas dalam perhitungan
neraca energi
- Proses ini tidak melibatkan kerja,
- Selesaikan terlebih dahulu neraca massa jika memungkinkan;
di dalam system tidak terjadi reaksi, maka
neraca massa total N1 = N2 = 100 mol/s
neraca massa komponen CH4 : 0,9(100) = YCH4,2 . N2
CO2 : 0,1(100) = YCO2,2 . N2
Didapatkan YCH4,2 = 90%
YCO2,2 = 10%
- Susunlah persamaan neraca energi :
Q = N2 [H2(T2) H2(Tref)] N1 [H1(T1) H1(Tref)]
Q = N2 [H2(293K) H2(Tref)] N1 [H1(311K) H1(Tref)]
- Tentukan harga Tref , misalkan kita ambil Tref = 298 K
H2(293K) H2(298K) = YCH4,2 Cp,CH4 dT + YCO2,2 Cp,CO2 dT
= 0,9(38,387)(293-298) + 0,1(19,022)(293-298)
= -182,2525 J/mol
H1(311K) H1(298K) = YCH4,1 Cp,CH4 dT + YCO2,1 Cp,CO2 dT
= 0,9(38,387)(311-298) + 0,1(19,022)(311-298)
= 473,8565 J/mol
Q = 100 (-182,2525) 100(473,8565) = -65610,9 J/s
Tugas :
Suatu aliran didinginkan dalam heat exchanger dari keadaan masuk dengan temperatur T1 = 38 C.
Laju alir gas alam adalah 100 mol/s. Karena suatu masalah teknis, kemampuan perpindahan
panas dalam heat exchanger ini turun menjadi 40.000 J/s (dari soal di atas 65.610,9 J/s).
Tentukan temperatur gas keluar heat exchanger, T2.
Contoh kasus:
Aliran gas proses pada temperatur 400 C akan didinginkan secara cepat menuju 200 C dengan
pendinginan secara langsung (direct quenching) dengan benzene cair dingin pada temperatur 20
C. Jika aliran gas proses terdiri atas 40% C6H6, 30% C6H5CH3, 10% CH4 dan 20% H2., hitunglah
laju alir benzene yang diperlukan untuk mendinginkan gas dengan laju alir 1000 kmol/jam,
asumsi bahwa proses berlangsung secara adiabatic.
Penyelesaian :
Jumlah variable
aliran
NM NME
Aliran 9 9
T,P 0 3
Q,W 0 2
Jumlah persamaan TTSL
Massa 4 4
Energi 0 1
Jumlah data yang diketahui
Komposisi 3 3
T,P 0 3
Q=0;W=0 0 2
Basis 1 1
Derajat
Kebebasan
1 0
Persmasalahan ini well specified, namun harus diselesaikan secara coupled antara persamaan
neraca massa dan neraca energi.
Persamaan neraca energi :
Q = N3[H3(473K) H3(Tref)] N1[H1(293K) H1(Tref)] N2[H2(673K) H2(Tref)]
Tref = T3 = 473 K
Maka,
0 = N3[H3(473K) H3(473)] N1[H1(293K) H1(473)] N2[H2(673K) H2(473)]
nol
N1[H1(293K) H1(473)] = N2[H2(673K) H2(473)] N1[H1(473K) H1(293)] = N2[H2(673K)
H2(473)]
Komponen Fasa Cp, J/mol.K
(disederhanakan)
C6H6 Gas (g) 18,587
C6H5CH3 Gas (g) 31,820
CH4 Gas (g) 38,387
H2 Gas (g) 17,639
C6H6 Cairan (l) -7,270
Panas dari Fase Transisi
Mengambil sampel fase I dan perlahan-lahan mengubahnya menjadi fase II. Beberapa panas
Q akan diserap.
- Karena ini adalah reversibel,
(1)
- Karena dalam kesetimbangan P 1 = P 2, proses terjadi pada tekanan konstan
- Karena T = 1 T 2, itu terjadi pada suhu konstan
Kami memiliki
atau
Panas dari fase transisi yang sama dengan perubahan entalpi.
Clapeyron-Clausius Formula
Hukum Umum
Di P - T diagram fase transisi terjadi di sepanjang garis P (T). Mari kita menghitung
bersinggungan dengan jalur ini dP / dT.
Potensi kimia sama:
Membedakan:
(2)
Kita tahu dari pelajaran-pelajaran sebelumnya yang
dan karena itu
dengan jumlah s dan v menjadi per molekul
Dari ( 2 ):
atau
Sejak
kami memperoleh
(3)
Ini adalah Clapeyron-Clausius persamaan
Konsekuensi
- Untuk gas cair transisi fase q> 0. Karena v 2> v 1, dT / dP = (dP / dT) -1> 0. Suhu
titik didih meningkat dengan tekanan
- Untuk padat-cair transisi fase q> 0 (kecuali: ). Biasanya v 2> v 1, dan
meningkatkan titik lebur dengan tekanan. Untuk air v 2 <v 1, dan menurun - itulah
sebabnya skating & ski adalah mungkin!
Contoh: Liquid-Gas Tahap Transisi
Asumsi:
1. Tahap transisi panas q tidak tergantung pada T dan P:
2. Gas ideal (PV = NKT), dan volumenya jauh parutan daripada cairan:
Kami memperoleh:
atau
Orde Fase Transisi
Jika kita bergerak dari fase I ke fase II, G potensial termodinamika kontinu (mengapa?), Tapi
melompat turunan pertama S. Kemungkinan lain: S kontinu, namun melompat.
Definisi:
jika turunan ke-n energi bebas
tidak berkelanjutan, dan semua turunannya lebih rendah tidak, transisi adalah n-th
order.
Kesetimbangan fasa:
urutan pertama fase transisi!
Fase transisi urutan kedua:
Curie titik, beberapa transisi fase kristal cair ...
Praktis panduan:
jika q = 0, transisi adalah urutan kedua (atau lebih tinggi!).
Pertama-order-close-to-orde kedua transisi:
q kecil (kristal cair)
ANALISIS SISTEM TAK BEREAKSI
Variabel-variabel Neraca Energi
Bentuk umum persamaan neraca energi dengan sistem terbuka dan alur masuk dan keluar
lebih dari satu adalah:
( ) ( )
|
.
|
\
|
|
.
|
\
|
=
j streams
outlet
k streams
inlet
k
2 k
j
2 j
v
2
1
+ gz + phase P, T, w, H F - v
2
1
+ gz + phase P, T, w, H F
dt
dW
-
dt
dQ
Pada persamaan tersebut, terdapat variabel yang sudah diketahui pada saat kita mempelajari
neraca massa, yaitu komposisi dan laju alir. Variabel yang baru kita kenal adalah temperatur,
tekanan, fase, elevasi, dan kecepatan, dan variabel sistem W dan Q.
Persamaan neraca energi dalam keadaan steady state pada sistem yang melibatkan S zat dapat
direduksi menjadi :
=
(
(
(
=
S
s 1
j streams
outlet
k streams
inlet
k k
s
j j
s
) Hs(T F - ) Hs(T F
dt
dW
-
dt
dQ
Sifat-sifat Persamaan Neraca Energi
Contoh soal 1
Dalam suatu turbin seperti pada contoh 7.14 Reklaitis, kondisi sisa panas yang ada
terspesifikasi menjadi 1 bar dan kualitas 0,9. Hitunglah laju umpan yang masuk per 1 hp
terproduksi dalam turbin.
Penyelesaian :
Dari gambar 7.5 Reklaitis, panas masuk dan keluar diketahui, elevasi dan kecepatan juga
diketahui, dan laju panas menjadi :
Btu/h 300F
dt
dQ
=
Persamaan neraca energinya menjadi :
( ) ( )
(
+ + =
2
2
4
1 2
10 1
2
1
200 300
s
ft
gc
ft
gc
g
H H F
dt
dW
F
Dimana,
kg kJ H / 01 , 2455 ) 5 , 417 ( 1 , 0 ) 4 , 2675 ( 9 , 0
2
= + =
Dan
kg kJ H / 2 , 2776
1
=
Jadi,
Btu/h 07 , 138 300 F
dt
dW
F =
Analisa Derajat Kebebasan
Pada umumnya, permasalahan neraca energi dengan satu unit tanpa reaksi kimia akan
melibatkan :
1. Variabel alur (temperatur dan laju alir zat) dan variabel unit (dQ/dt dan dW/dt).
2. Persamaan neraca massa.
3. Satu persamaan neraca energi.
4. Spesifikasi permasalahan (termasuk spesifikasi temperatur dan kemungkinan
dQ/dt, dW/dt).
5. Basis perhitungan.
Permasalahan neraca energi bisa saja diartikan sebagai permasalahan neraca massa dengan satu
tambahan persamaan, neraca energi, dan beberapa tambahan variabel, alur temperatur dan unit dW/dt,
variabel dQ/dt.
Contoh soal 2:
Buatlah analisis derajat kebebasan pada problem 7.25 Reklaitis.
C6H6
T = 20
0
C
Quench
Penyelesaian:
Dari gambar, terlihat bahwa problem melibatkan 3 alur dan tidak ada transfer energi sebagai
panas atau kerja. Alur 2 dan 3 masing-masing melibatkan 4 alur zat ditambah temperatur.
Alur 1 melibatkan satu alur zat ditambah temperatur. Dapat dibuat 4 persamaan neraca massa
dan 1 persamaan neraca energi. Variabel T, dQ/dt dan dW/dt semuanya terspesifikasi. Tabel
derajat kebebasannya adalah :
Jumlah variabel
Variabel Alur 9
Ts 3
dQ/dt,dW/dt 2
14
Jumlah neraca
Massa 4
Energi 1
5
Jumlah terspesifikasi
Komposisi 3
Temperatur 3
dQ/dt, dW/dt=0 2
8
Basis 1
Derajat Kebebasan 0
Hot gas
C6H6 0,4
C6H5CH3 0,3
CH4 0,1
H2 0,2
T = 400
0
C
All vapor
Q = 0
C6H6
C6H5CH3
CH4
H2
T = 200
0
C
All vapor
PENYELESAIAN PEMICU
Problem 6.16 Reklaitis
Persamaan tekanan uap untuk sebuah zat adalah :
Dimana p dalam psia dan t dalam F.
a. Tentukan nilai tetapan A,B, dan C dalam persamaan dimana tekanan dalam kPa dan
temperatur dalam K:
()
b. Verifikasi konversi dengan mengevaluasi kedua persamaan jika diketahui p = 100
psia dan T = 212 F.
Penyelesaian :
a.
Misal : t = 100 F
Pada T = 100 F, p = 0,1353 psia
37,78 C = 37,78 + 273,15 K = 310,93 K
p = 0,1353 psia x 6,89476 kPa/1 psia = 0,9329 kPa
jadi, pada T = 310,93 K, p = 0,9329 kPa
Misal : t = 200 F
Pada T = 200 F, p = 1 psia
93,33 C = 93,33 + 273,15 K = 366,48 K
p = 1 psia x 6,89476 kPa/1 psia = 6,89476 kPa
jadi, pada T = 366,48 K, p = 6,89476 kPa
Misal : t = 300 F
Pada T = 300 F, p = 4,173 psia
148,89 C = 148,89 + 273,15 K = 422,04 K
p = 4,173 psia x 6,89476 kPa/1 psia = 28,7718 kPa
jadi, pada T = 422,04 K, p = 28,7718 kPa
Eliminasi persamaan (1) dan (2)
Eliminasi persamaan (2) dan (3)
Eliminasi persamaan (4) dan (5)
Masukkan nilai A dan C yang diperoleh ke dalam persamaan (1) untuk memperoleh nilai B :
Persamaannya menjadi :
b. Verifikasi I
p = 100 psia
p = 100 psia x 6,89476 kPa/1 psia = 689,476 kPa
T(C) = 651,123 - 273,15 = 377,97 C
Pada p = 100 psia, t = 712 F Terbukti
Pada p = 689,476 kPa, t = 712 F
Verifikasi II
Pada t = 212 F
T = 212 F
100 C = 100 + 273,15 K = 373,15 K
1 psia = 6,89476 kPa
8,384 kPa x 1 psia/6,89476 kPa = 1,22 psia
Pada t = 212 F, p = 1,22 psia
Pada t = 373,15 K, p = 1,22 psia Terbukti
Problem 7.25 Reklaitis
Evaporator merupakan spesial tipe dari heat exchanger dimana uap panas digunakan untuk
memanaskan larutan hingga mendidihkan sebagian dari pelarutnya. Pada evaporator seperti
terlihat pada gambar, larutan garam terdiri dari 1 wt % garam dalam air diumpankan pada
tekanan 1 bar dan 50 C. Larutan garam yang keluar dari evaporator mengandung 2 wt% dan
merupakan saturated liquid pada tekanan 1 bar. Air yang diuapkan merupakan saturated
steam pada 1 bar. Jika saturated steam pada 2 bar digunakan sebagai sumber panas dan
kondensatnya diasumsikan saturated liquid pada 2 bar, hitunglah kilogram dari 2 bar uap
yang dibutuhkan per kilogram uap air yang dihasilkan . Diasumsikan larutan garam
mempunyai sifat-sifat seperti liquid water.
Penyelesaian :
Dari tabel superheated steam, pada 1 bar dan 50 C, = 209,3 kJ/kg
Dari tabel, saturated water pada 1 bar, = 417,5 kJ/kg
Dari tabel, saturated steam pada 1 bar, = 2675,4 kJ/kg
Dari tabel, saturated steam pada 2 bar = 2706,3 kJ/kg
Dari tabel, saturated water pada 2 bar = 504,7 kJ/kg
1 % Brine
1 bar
50C
Saturated steam 2 bar Saturated condensate 2 bar
2 % Brine
1 bar
(saturated liquid)
Saturated steam 1 bar
1
2
3
4
5
Basis : 100 kg
- Karakteristik sistem adalah sistem terbuka (open system), ada zat yang masuk,
melewati dan keluar dari sistem.
- Sistem terdiri dari 2 komponen yaitu air dan garam
- Proses yang terjadi pada sistem merupakan isobarik, yaitu berada pada tekanan
konstan.
Neraca total
jumlah energi masuk = jumlah energi keluar + akumulasi energi dalam sistem
m
1
= 100 kg
0,02 x m
3
= 1 kg
m
3
= 50 kg
m
1
= m
2
+ m
3
m
2
= 100 - 50 = 50 kg
m
4
= m
5
, karena sistem hanya memberi panas
1
= 209,3 kJ/kg
2
= 2675,4 kJ/kg
3
= 417,5 kJ/kg
4
= 2706,3 kJ/kg
5
= 504,7 kJ/kg
Masukkan nilai-nilai ke dalam persamaan :
1 . 209,3 + 99 . 209,3 + m
4
. 2706,3 = 50 . 2675,4 + 1 . 417,5 + 49 . 417,5 + m
4
. 504,7
209,3 + 20720,7 + 2706,3m
4
= 133770 + 417,5 + 20457,5 + 504,7m
4
2201,6m
4
= 133715
m
4
= 60,74 kg
jadi, m
4
: m
2
= 60,74 : 50 = 1,2147
garam :1 kg
air : 99 kg
2 bar
1 bar
(saturated water)
1 3
4
5
Saturated steam 1 bar
2
saturated steam
2 bar
saturated condensate
(water)
1 bar
50 C
garam : 2%
air : 98%
Problem 7.44 Reklaitis
Pada proses asetat anhidrat, 100 mol/jam sebuah alur proses terdiri dari 4% ketena, 10% asam
asetat, 43% metana, dan 43% karbon dioksida (dalam % mol) pada 700 C dan akan
didinginkan menjadi 400 C dengan direct quenching menggunakan asam asetat glasial cair
pada 50 C.
a. Dengan menggunka data berikut ini, hitunglah alur asam asetat yang dibutuhkan dan
komposisi gas yang didinginkan.
Kapasitas Panas Gas (cal/gmol . K)
a b x 10
2
c x 10
5
d x 10
9
CH
4
4,750 1,2 0,303 -2,63
CO
2
6,393 1,01 -0,3405 -
CH
3
COOH 8,20 4,805 -3,056 8,31
CH
2
O 4,11 2,966 -1,793 4,72
H
VL
(CH
3
COOH,391,4 K) = 5,83 kcal/gmol
Mean C
p
(CH
3
COOH, cair) = 36 cal/gmol . K
b. Misalkan terspesifikasi 40 mol/jam asam asetat digunakan sebagai. Hitung suhu
keluaran gas.
Penyelesaian :
(a)
4 % CH
2
O
(g)
10% CH
3
COOH
(g)
43% CH
4 (g)
43% CO
2 (g)
N = 100 mol/jam
T= 700
o
C
(1)
CH
3
COOH
(l)
T= 50
o
C
(2)
CH
2
O
(g)
CH
3
COOH
(g)
CH
4 (g)
CO
2 (g)
T= 400
o
C
(3)
Temperature referensi = 400
o
C = 673,15K
Neraca energi
Panas masuk = panas keluar
( )
} } }
}
=
|
|
.
|
\
|
+ +
K 15 , 73 6
K 15 , 73 6
323,15K
391,4K
l vl
391,4K
673,15K
v 2
K 15 , 73 9
673,15K
CpdT N dT Cp 391,4K H dT Cp N CpdT N
( ) 0 dT Cp 391,4K H dT Cp N CpdT N
323,15K
391,4K
l vl
391,4K
673,15K
v 2
973,15K
973,15K
=
|
|
.
|
\
|
+ +
} }
}
( )
|
|
.
|
\
|
+ =
} }
}
323,15K
391,4K
l vl
391,4K
673,15K
v 2
973,15K
673,15K
dT Cp 391,4K H dT Cp N CpdT N
( )
|
|
.
|
\
|
+ + =
} }
}
391,4K
323,15K
l vl
673,15K
391,4K
v 2
973,15K
673,15K
dT Cp 391,4K H dT Cp N CpdT N
Tinjau masing-masing komponen Alur 1
CH
2
O
a= 4,11
b = 2,96610-2
c=-1,79310-5
d=4,7210-9
NCH
2
O = 4%100 mol/h = 4 mol/h
Panas CH
2
O ( )
}
+ + =
973,15K
673,15K
3 9 2 5 2
CH2O
dT T 10 4,72 T 10 1,793 T 10 2,966 4,11 N
( )
}
+ + =
973,15K
673,15K
3 9 2 5 2
dT T 10 4,72 T 10 1,793 T 10 2,966 4,11 4mol/h
973,15
673,15
4 9 3 5 2 2
T 10 4,72 0,25 T 10 1,793
3
1
T 10 2,966 0,5 4,11T 4mol/h
|
.
|
\
|
+ + =
=22753,44 cal/h
CH
3
COOH
a= 8,20
b = 4,80510-2
c=-3,05610-5
d=8,3110-9
NCH
3
COOH = 10%100 mol/h = 10 mol/h
Panas CH
3
COOH
( )
}
+ + =
973,15K
673,15K
3 9 2 5 2
CH3COOH
dT T 10 8,31 T 10 3,056 T 10 4,805 8,20 N
( )
}
+ + =
973,15K
673,15K
3 9 2 5 2
dT T 10 8,31 T 10 3,056 T 10 4,805 8,20 10mol/h
973,15
673,15
4 9 3 5 2 2
T 10 8,31 0,25 T 10 3,056
3
1
T 10 4,805 0,5 8,20T 10mol/h
|
.
|
\
|
+ + =
=94815,66 cal/h
CH
4
a= 4,75
b = 1,210-2
c=0,30310-5
d=-2,6310-9
NCH
4
= 43%100 mol/h = 43 mol/h
Panas CH
4
( )
}
+ + =
973,15K
673,15K
3 9 2 5 2
CH4
dT T 10 2,63 T 10 0,303 T 10 1,2 4,75 N
( )
}
+ + =
973,15K
673,15K
3 9 2 5 2
dT T 10 2,63 T 10 0,303 T 10 1,2 4,75 43mol/h
973,15
673,15
4 9 3 5 2 2
T 10 2,63 0,25 T 10 0,303
3
1
T 10 1,2 0,5 4,75T 43mol/h
|
.
|
\
|
+ + =
=195925,16 cal/h
CO
2
a= 6,393
b = 1,0110-2
c=-0,340510-5
d=0
NCO
2
= 43%100 mol/h = 43 mol/h
Panas CO
2
( )
}
+ =
973,15K
673,15K
2 5 2
CO2
dT T 10 0,3405 T 10 1,01 6,393 N
( )
}
+ =
973,15K
673,15K
2 5 2
dT T 10 0,3405 T 10 1,01 6,393 43mol/h
973,15
675,13
3 5 2 2
T 10 0,3405
3
1
T 10 1,01 0,5 6,393T 43mol/h
|
.
|
\
|
+ =
=159626,30 cal/h
Panas total alur 1,
cal/h 55 , 73120 4 159626,30 195925,16 94815,66 22753,44 CpdT N
C 700
C 400
o
o
= + + + =
}
Alur 2
( )
|
|
.
|
\
|
+ +
} }
391,4K
323,15K
l vl
673,15K
391,4K
v 2
dT Cp 391,4K H dT Cp N
mean Cp (CH3COOH, liquid) = 36 cal/mol.K
}
391,4K
323,15K
l
dT Cp = (391,4 323,15)36= 2457 cal/mol
Hvl = 5830 cal/mol
=
}
673,15K
391,4K
v
dT Cp ( )
}
+ +
673,15K
391,4K
3 9 2 5 2
dT T 10 8,31 T 10 3,056 T 10 4,805 8,20
=
}
673,15K
391,4K
v
dT Cp
673,15
391,4
4 9 3 5 2 2
T 10 8,31 0,25 T 10 3,056
3
1
T 10 4,805 0,5 8,20T
|
.
|
\
|
+ +
=
}
673,15K
391,4K
v
dT Cp 7397,75 cal/mol
Neraca energi
( )
|
|
.
|
\
|
+ + =
} }
}
391,4K
323,15K
l vl
673,15K
391,4K
v 2
973,15K
673,15K
dT Cp 391,4K H dT Cp N CpdT N
( ) cal/mol 2457 cal/mol 5830 cal/mol 7397,75 N cal/h 55 , 73120 4
2
+ + =
( ) cal/mol 15684,75 N cal/h 55 , 73120 4
2
=
Laju alir asam asetat pada alur 2,
mol/h 1644 , 30
cal/mol 15684,75
cal/h 55 , 73120 4
N
2
= =
(b)
4 % CH
2
O
(g)
10% CH
3
COOH
(g)
43% CH
4 (g)
43% CO
2 (g)
N = 100 mol/jam
T= 700
o
C
(1)
CH
3
COOH
(l)
=40mol/h
T= 50
o
C
(2)
CH
2
O
(g)
=4mol/h
CH
3
COOH
(g)
=50 mol/h
CH
4 (g)
=43mol/h
CO
2 (g)
=43mol/h
T= ?
o
C
(3)
Ambil temperature referensi =700
o
C=973,15 K
Panas masuk = panas keluar
( )
} } }
}
=
|
|
.
|
\
|
+ +
K ?
K 15 , 73 9
323,15K
391,4K
l vl
391,4K
973,15K
v 2
K 15 , 73 9
973,15K
CpdT N dT Cp 391,4K H dT Cp N CpdT N
( )
} } }
=
|
|
.
|
\
|
+
K ?
K 15 , 73 9
323,15K
391,4K
l vl
391,4K
973,15K
v 2
CpdT N dT Cp 391,4K H dT Cp N
Tinjau alur 2
N2 = 40 mol/h
}
391,4K
973,15K
v
dT Cp = ( )
}
+ +
391,4K
973,15K
3 9 2 5 2
dT T 10 8,31 T 10 3,056 T 10 4,805 8,20
}
391,4K
973,15K
v
dT Cp =
391,4
973,15
4 9 3 5 2 2
T 10 8,31 0,25 T 10 3,056
3
1
T 10 4,805 0,5 8,20T
|
.
|
\
|
+ +
}
391,4K
973,15K
v
dT Cp = 16879,32 cal/mol
}
323,15K
391,4K
l
dT Cp = (323,15 391,4)36= 2457 cal/mol
Hvl = 5830 cal/mol
( ) ( ) cal/mol 2457 cal/mol 5830 cal/mol 16879,32 mol 40 dT Cp 391,4K H dT Cp N
323,15K
391,4K
l vl
391,4K
973,15K
v 2
=
|
|
.
|
\
|
+
} }
( ) cal/h 1006652,76 dT Cp 391,4K H dT Cp N
323,15K
391,4K
l vl
391,4K
973,15K
v 2
=
|
|
.
|
\
|
+
} }
Tinjau masing-masing komponen Alur 3
CH2O
a= 4,11
b = 2,96610-2
c=-1,79310-5
d=4,7210-9
NCH2O = 4 mol/h
Panas CH2O ( )
}
+ + =
?K
973,15K
3 9 2 5 2
CH2O
dT T 10 4,72 T 10 1,793 T 10 2,966 4,11 N
( )
}
+ + =
?K
973,15K
3 9 2 5 2
dT T 10 4,72 T 10 1,793 T 10 2,966 4,11 4mol/h
X
973,15
4 9 3 5 2 2
T 10 4,72 0,25 T 10 1,793
3
1
T 10 2,966 0,5 4,11T 4mol/h
|
.
|
\
|
+ + =
=16,44 (X-973,15)+0,0593(X2-973,152)-2,390710-5(X3-973,153)+ 4,7210-5(X4-
973,154)
CH3COOH
a= 8,20
b = 4,80510-2
c=-3,05610-5
d=8,3110-9
NCH3COOH = 50 mol/h
Panas CH3COOH
( )
}
+ + =
?K
973,15K
3 9 2 5 2
CH3COOH
dT T 10 8,31 T 10 3,056 T 10 4,805 8,20 N
( )
}
+ + =
?K
973,15K
3 9 2 5 2
dT T 10 8,31 T 10 3,056 T 10 4,805 8,20 50mol/h
X
973,15
4 9 3 5 2 2
T 10 8,31 0,25 T 10 3,056
3
1
T 10 4,805 0,5 8,20T 50mol/h
|
.
|
\
|
+ + =
= 410(X-973,15)+1,20125(X2-973,152)-0,0005(X3-973,153)+1,0387 10-7(X4-973,154)
CH4
a= 4,75
b = 1,210-2
c=0,30310-5
d=-2,6310-9
NCH4 = 43 mol/h
Panas CH4
( )
}
+ + =
?K
973,15K
3 9 2 5 2
CH4
dT T 10 2,63 T 10 0,303 T 10 1,2 4,75 N
( )
}
+ + =
?K
973,15K
3 9 2 5 2
dT T 10 2,63 T 10 0,303 T 10 1,2 4,75 43mol/h
X
973,15
4 9 3 5 2 2
T 10 2,63 0,25 T 10 0,303
3
1
T 10 1,2 0,5 4,75T 43mol/h
|
.
|
\
|
+ + =
= 204,25(X-973,15)+0,258(X2-973,152)+4,34310-5(X3-973,153)-2,827210-5(X4-
973,154)
CO2
a= 6,393
b = 1,0110-2
c=-0,340510-5
d=0
NCO2 = 43 mol/h
Panas CO2
( )
}
+ =
?K
973,15K
2 5 2
CO2
dT T 10 0,3405 T 10 1,01 6,393 N
( )
}
+ =
?K
973,15K
2 5 2
dT T 10 0,3405 T 10 1,01 6,393 43mol/h
X
973,15
3 5 2 2
T 10 0,3405
3
1
T 10 1,01 0,5 6,393T 43mol/h
|
.
|
\
|
+ =
=274,899(X-973,15)+0,2175(X2-973,152)+4,88010-5(X3-973,153)
Jumlahkan
16,44 (X-973,15) +0,0593(X2-973,152) -2,390710-5(X3-973,153) + 4,7210-5(X4-
973,154)
410(X-973,15) +1,20125(X2-973,152) -0,0005(X3-973,153) +1,0387 10-7(X4-
973,154)
204,25(X-973,15) +0,258(X2-973,152) +4,34310-5(X3-973,153) -2,827210-5(X4-
973,154)
274,899(X-973,15) +0,2175(X2-973,152) +4,88010-5 (X3-973,153)
+
905,589(X-973,15) +1,7357(X2-973,152) -0,00054(X3-973,153) +8,0310-8(X4-
973,154)
( )
} } }
=
|
|
.
|
\
|
+
K ?
K 15 , 73 9
323,15K
391,4K
l vl
391,4K
973,15K
v 2
CpdT N dT Cp 391,4K H dT Cp N
cal/h 1006652,76 =905,589(X-973,15)+1,7357(X2-973,152)-0,00054(X3-
973,153)+8,0310-8(X4-973,154)
X=612,7632 K = 339,6132
o
C
You might also like
- AattkkkDocument30 pagesAattkkkRoiiiikkkkNo ratings yet
- 1 MTK Konsep Neraca MasaDocument23 pages1 MTK Konsep Neraca MasaPermana PakpahanNo ratings yet
- Soal Latihan 1Document2 pagesSoal Latihan 1hana faqihNo ratings yet
- Viii Sistem Rektor AlirDocument11 pagesViii Sistem Rektor AlirAhmad-JR- habibieNo ratings yet
- Lapres 1 Sesi 3Document26 pagesLapres 1 Sesi 3yudha7wira7rahmanNo ratings yet
- 4 Bab III Neraca Massa Dengan Reaksi KimiaDocument6 pages4 Bab III Neraca Massa Dengan Reaksi KimiaROMANo ratings yet
- Perpindahan Massa Dan Difusi RevDocument65 pagesPerpindahan Massa Dan Difusi RevalgoNo ratings yet
- Aplikasi Industri Teknik BioprosesDocument3 pagesAplikasi Industri Teknik BioprosesFrans N SNo ratings yet
- Konduktivitas dan Titrasi KonduktometriDocument4 pagesKonduktivitas dan Titrasi KonduktometriAyu NurpitrianiNo ratings yet
- Thermo Soal Bab 4Document9 pagesThermo Soal Bab 4Nur Azisah100% (1)
- Laporan Praktikum Tangki Berpengaduk Bab IIIDocument22 pagesLaporan Praktikum Tangki Berpengaduk Bab IIIfauziputraNo ratings yet
- Variabel-Variabel Proses KimiaDocument52 pagesVariabel-Variabel Proses KimiaElisDianaUlfaNo ratings yet
- Jawaban No. 3 Termo Pemicu 4Document7 pagesJawaban No. 3 Termo Pemicu 4Ade Sari TrianaNo ratings yet
- OPTIMASI PERSAMAAN KONTINUITASDocument15 pagesOPTIMASI PERSAMAAN KONTINUITASega assyifaNo ratings yet
- FugasitasKelompok ReferensiDocument13 pagesFugasitasKelompok ReferensiVLädD.ÄLdzNo ratings yet
- Identifikasi Kimia OrganikDocument14 pagesIdentifikasi Kimia OrganikRahmat HidayatNo ratings yet
- Koefisien DifusiDocument10 pagesKoefisien DifusiAhmad SodikinNo ratings yet
- Modul 3Document12 pagesModul 3xolo jNo ratings yet
- Perhitungan Panas Penguapan dan Perubahan EntalpiDocument14 pagesPerhitungan Panas Penguapan dan Perubahan EntalpiGandrig F VendrisNo ratings yet
- Neraca Energi Tanpa Reaksi - Sistem Multikomponen Analisis Derajat KebebasanDocument12 pagesNeraca Energi Tanpa Reaksi - Sistem Multikomponen Analisis Derajat KebebasanMitha AmaliaNo ratings yet
- HEAT EXCHANGER TEORIDocument5 pagesHEAT EXCHANGER TEORIgisNo ratings yet
- Pertemuan Ke-4NM (Producer Gas Dan MetilYodida)Document13 pagesPertemuan Ke-4NM (Producer Gas Dan MetilYodida)GilmanNo ratings yet
- ToDocument25 pagesToMuhammad Dzikri Ajauhari100% (1)
- Materi 4 Kelompok Tak BerdimensiDocument9 pagesMateri 4 Kelompok Tak Berdimensisalma rahmaNo ratings yet
- 5.1 Reaksi Jamak 1Document10 pages5.1 Reaksi Jamak 1primadya pradiptaNo ratings yet
- Fenomena Perpindahan Massa, Panas, dan MomentumDocument15 pagesFenomena Perpindahan Massa, Panas, dan Momentumdewilestari6372No ratings yet
- Laporan Praktikum Operasi Teknik Kimia Karakteristik Pompa Dan KavitasiDocument44 pagesLaporan Praktikum Operasi Teknik Kimia Karakteristik Pompa Dan KavitasiAchri Isnan KhamilNo ratings yet
- Tugas Pengendalian Proses (Alat Industri & Alat Pengukuran)Document13 pagesTugas Pengendalian Proses (Alat Industri & Alat Pengukuran)Italiana HakimNo ratings yet
- 7-NM Dengan ReaksiDocument13 pages7-NM Dengan ReaksiseptianaNo ratings yet
- ViskositasDocument30 pagesViskositasmade ayuNo ratings yet
- 3 - Proses Dan Variabel ProsesDocument46 pages3 - Proses Dan Variabel ProsesAnnisa IstiqomahNo ratings yet
- Contoh Soal MtkimDocument5 pagesContoh Soal Mtkimlita saf100% (1)
- FLUID FRICTIONDocument15 pagesFLUID FRICTIONAbid ShinraNo ratings yet
- Kul Humidifikasi 2Document20 pagesKul Humidifikasi 2Ly2n_cuteNo ratings yet
- Azaz Teknik KimiaDocument42 pagesAzaz Teknik KimiaJuneeNo ratings yet
- PFR KinetikaDocument22 pagesPFR KinetikaJianNo ratings yet
- NERACA REAKSIDocument5 pagesNERACA REAKSIMuhammad WendyNo ratings yet
- Tugas KontrolDocument84 pagesTugas KontrolArsyilah Nurqolbiah MursyidNo ratings yet
- MTKDocument279 pagesMTKannisa sabrilaNo ratings yet
- Pencegahan HidratDocument27 pagesPencegahan HidratZeus WooNo ratings yet
- Persamaan Arrhenius Dan Energi AktivasiDocument11 pagesPersamaan Arrhenius Dan Energi Aktivasiav_treeNo ratings yet
- Laporan MixingDocument2 pagesLaporan MixingfaridaNo ratings yet
- BAB-5 Reaktor Ideal TunggalDocument18 pagesBAB-5 Reaktor Ideal TunggalDimas Rian SaputraNo ratings yet
- Perbedaan kerja dan panasDocument3 pagesPerbedaan kerja dan panasFajar PratamaNo ratings yet
- Pertemuan 5 NeracaDocument35 pagesPertemuan 5 NeracaAndri Nur RizkyNo ratings yet
- LARUTAN IDEALDocument73 pagesLARUTAN IDEALFemi Juana Putri GintingNo ratings yet
- Pengertian Saturated SteamDocument4 pagesPengertian Saturated SteamNasrul ZA ST MTNo ratings yet
- Kuc 1Document45 pagesKuc 1Kagak Ajek100% (1)
- Neraca Massa Dengan Banyak Unit ProsesDocument20 pagesNeraca Massa Dengan Banyak Unit ProsesalmengarunNo ratings yet
- Tugas Ekonomi TeknikDocument11 pagesTugas Ekonomi TeknikDhea Kana ZhafiraNo ratings yet
- Reaktor 1 Dan 2Document112 pagesReaktor 1 Dan 2yayagustiNo ratings yet
- REAKSI KIMIADocument13 pagesREAKSI KIMIAseptianaNo ratings yet
- Refrigeration and LiquefactionDocument11 pagesRefrigeration and LiquefactionngaosNo ratings yet
- TK2202 - Teknik Reaksi Kimia IDocument29 pagesTK2202 - Teknik Reaksi Kimia Ifebri setyawanNo ratings yet
- Lapres5 - 19031010029 - Cindy Saskia Damayanti - A2Document32 pagesLapres5 - 19031010029 - Cindy Saskia Damayanti - A2Saskia damayantiNo ratings yet
- Fistat KelompokDocument23 pagesFistat KelompokNurul Elnica0% (1)
- TERMODINAMIKA DASARDocument4 pagesTERMODINAMIKA DASARNurul Elnica100% (2)
- Sistem Termodinamika dan Spesifikasi KeadaannyaDocument4 pagesSistem Termodinamika dan Spesifikasi KeadaannyaAyuu Suurya AguustinNo ratings yet
- Rizka Fitriana Ayundari - Materi Konsep Dasar TermodinamikaDocument5 pagesRizka Fitriana Ayundari - Materi Konsep Dasar TermodinamikaRizka Fitriana ANo ratings yet
- Cara Mendownload Jurnal Internasional BerbayarDocument1 pageCara Mendownload Jurnal Internasional BerbayarTika RisyadNo ratings yet
- Pengetahuan Lingkungan (Ringkasan Hal 19-41)Document13 pagesPengetahuan Lingkungan (Ringkasan Hal 19-41)Tika RisyadNo ratings yet
- TURBIN DAN EKSPANDERDocument5 pagesTURBIN DAN EKSPANDERTika RisyadNo ratings yet
- Neraca Massa Sistem Tak-BereaksiDocument103 pagesNeraca Massa Sistem Tak-BereaksiTika RisyadNo ratings yet
- EKSTRAKSI FLAVONOIDDocument8 pagesEKSTRAKSI FLAVONOIDTika RisyadNo ratings yet
- BAB II Pemicu 7Document6 pagesBAB II Pemicu 7Tika RisyadNo ratings yet
- 1.menjadi WirausahaDocument2 pages1.menjadi WirausahaTika RisyadNo ratings yet
- Tugas Kelompok BioseparasiDocument8 pagesTugas Kelompok BioseparasiTika RisyadNo ratings yet
- Tugas TK3Document28 pagesTugas TK3Tika RisyadNo ratings yet
- Kecelakaan KerjaDocument29 pagesKecelakaan KerjaTika Risyad100% (3)
- Paper tk3Document12 pagesPaper tk3Tika RisyadNo ratings yet
- Kebisingan Full VersionDocument24 pagesKebisingan Full VersionTika RisyadNo ratings yet
- Makalah SulfonasiDocument8 pagesMakalah SulfonasiTika RisyadNo ratings yet
- AmdalDocument11 pagesAmdalTika RisyadNo ratings yet
- Presentasi TK3Document28 pagesPresentasi TK3Tika RisyadNo ratings yet
- Bab II Tinjauan Pustaka KRDocument6 pagesBab II Tinjauan Pustaka KRTika RisyadNo ratings yet
- Proses Pembuatan FormalinDocument3 pagesProses Pembuatan FormalinTika Risyad100% (1)
- PencernaanDocument9 pagesPencernaanTika RisyadNo ratings yet
- Isi PPGDocument16 pagesIsi PPGTika RisyadNo ratings yet
- Lampiran BDocument9 pagesLampiran BTika RisyadNo ratings yet
- BAB III Pemicu 4Document2 pagesBAB III Pemicu 4Tika RisyadNo ratings yet
- PPM Dan SterilisasiDocument23 pagesPPM Dan SterilisasiTika RisyadNo ratings yet
- Analisa RegresiDocument5 pagesAnalisa RegresiTika RisyadNo ratings yet
- Bab III Metodologi Percobaan KRDocument5 pagesBab III Metodologi Percobaan KRTika RisyadNo ratings yet
- BAB III KualitatifDocument12 pagesBAB III KualitatifTika Risyad100% (1)
- Tugas REGRESIDocument3 pagesTugas REGRESITika RisyadNo ratings yet
- Perbedaan Adalah RahmatDocument2 pagesPerbedaan Adalah RahmatTika RisyadNo ratings yet
- Bab IV BMDocument4 pagesBab IV BMTika RisyadNo ratings yet
- Tugas UtsDocument4 pagesTugas UtsTika Risyad0% (1)
- Tugas ResponsiDocument9 pagesTugas ResponsiTika RisyadNo ratings yet