Professional Documents
Culture Documents
Rumus-Rumus Termodinamika
Uploaded by
Elsya Dhana AlfiraOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Rumus-Rumus Termodinamika
Uploaded by
Elsya Dhana AlfiraCopyright:
Available Formats
Rumus-Rumus Fisika Lengkap/Termodinamika
Subbagian ini akan menjelaskan rumus-rumus Hukum Pertama Termodinamika
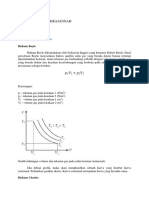
Hukum Pertama Termodinamika
Perubahan energi dalam: Keterangan:
:Perubahan energi dalam Nm (Joule) U2:Energi dalam pada keadaan akhir Nm (Joule) U1:Energi dalam pada keadaan awal (Joule)
Usaha yang dilakukan oleh gas pada tekanan tetap:
Keterangan:
p: Besarnya tekanan
N/m2
: Perubahan volume m3
Rumus umum usaha yang dilakukan gas: Penghitungan energi dalam:
Gas monoatomik:
Gas diatomik:
Proses-proses termodinamika gas
Proses isobarik (tekanan tetap)
1.
Diagram proses isobarik. Daerah berwarna kuning sama dengan usaha yang dilakukan. Proses isobarik adalah perubahan keadaan gas pada tekanan tetap.
Persamaan keadaan isobarik: Usaha yang dilakukan pada keadaan isobarik:
2.
Proses isokhorik (volume tetap)
Digram proses isokhorik. Grafiknya berupa garis lurus vertikal karena volumenya tidak berubah. Tidak ada usaha yang dilakukan pada proses isokhorik. Proses isokhorik adalah perubahan keadaan gas pada volume tetap.
Persamaan keadaan isokhorik:
3.
Proses isotermis/isotermik (temperature tetap)
Proses isotermik. Daerah berwarna biru menunjukkan besarnya usaha yang dilakukan gas. Proses isotermik adalah perubahan keadaan gas pada suhu tetap. Persamaan keadaan isotermik:
Usaha yang dilakukan pada keadaan isotermik:
Dari persamaan gas ideal
Rumus umum usaha yang dilakukan gas:
maka:
karena
bernilai tetap, maka:
Ingat integral ini!
maka persamaan di atas menjadi
maka menjadi:
4. Proses adiabatik (proses tanpa perpindahan panas)
Penyataan Proses adiabatik. Warna biru muda menunjukkan besarnya usaha yang dilakukan. Proses adiabatik adalah perubahan keadaan gas dimana tidak ada kalor yang masuk maupun keluar dari sistem.
Persamaan keadaan adiabatik: disebut eksponen adiabatis Tetapan Laplace:
karena maka persamaan diatas dapat juga ditulis:
Usaha yang dilakukan pada proses adiabatik:
You might also like
- JUDULDocument24 pagesJUDULFitriana Budi RizqiNo ratings yet
- SOAL LATIHAN TRY OUTDocument10 pagesSOAL LATIHAN TRY OUTBrian SteveNo ratings yet
- SOAL_PILIHAN_GANDADocument9 pagesSOAL_PILIHAN_GANDAanjar pamungkas100% (1)
- Biologi 1 UtbkDocument21 pagesBiologi 1 Utbkmudji irianikNo ratings yet
- Bab 2 Fluida 44-53Document11 pagesBab 2 Fluida 44-53Anonymous s7xTz1No ratings yet
- Kumpulan Soal Dan PembahasannyaDocument4 pagesKumpulan Soal Dan PembahasannyaZacky Rizaldy67% (3)
- Mesin Carnot P-VDocument3 pagesMesin Carnot P-Vsri f. RahmwatiNo ratings yet
- Nama Mineral PDFDocument1 pageNama Mineral PDFPandji AhmadNo ratings yet
- RUMUS FISIKADocument2 pagesRUMUS FISIKANafta PutraNo ratings yet
- Solusi Ujian 2 FI1101 26112016 - 1Document9 pagesSolusi Ujian 2 FI1101 26112016 - 1Jeremy GavrielNo ratings yet
- Soal Dan Kunci Jawaban Bidang Kimia - Try Out OSN-K PPSN 2024Document25 pagesSoal Dan Kunci Jawaban Bidang Kimia - Try Out OSN-K PPSN 2024mazayahisyamiNo ratings yet
- Soal Dan Kunci Olimpiade Kimia Siswa SMA SCE 2017 PDFDocument5 pagesSoal Dan Kunci Olimpiade Kimia Siswa SMA SCE 2017 PDFMay Sarii PandianganNo ratings yet
- Gerak MelingkarDocument11 pagesGerak MelingkarErickMartinSNo ratings yet
- SEMU HUKUM MENDELDocument8 pagesSEMU HUKUM MENDELZulfaa ZahidahNo ratings yet
- Soal dan Pembahasan UN Kimia SMA Tahun 2017Document31 pagesSoal dan Pembahasan UN Kimia SMA Tahun 2017Gavin Toy ArtNo ratings yet
- Pengukuran Fisika dan BesaranDocument2 pagesPengukuran Fisika dan BesaranFathul AzisNo ratings yet
- Soal Soal TermokimiaDocument3 pagesSoal Soal Termokimiaagil hidayah0% (1)
- Bab7 Momentum Dan ImpulsDocument24 pagesBab7 Momentum Dan Impulsdwi sakti prastyoNo ratings yet
- GLBBDocument11 pagesGLBBSyafinatul HidayahNo ratings yet
- TERMODINAMIKADocument22 pagesTERMODINAMIKAFahmi YahyaNo ratings yet
- Optimized Titles for Chemistry DocumentsDocument7 pagesOptimized Titles for Chemistry DocumentsAndina FathiyaturahmaNo ratings yet
- Soal Ulangan Laju ReaksiDocument10 pagesSoal Ulangan Laju ReaksiShinta YulianaNo ratings yet
- Peluang - IPADocument7 pagesPeluang - IPAHeru CahyadiNo ratings yet
- Siklus OTTO Dan DIESEL Ideal BerbedaDocument5 pagesSiklus OTTO Dan DIESEL Ideal BerbedaPandu Tri HanantoNo ratings yet
- ContentDocument48 pagesContentdudi ariyadiNo ratings yet
- SOAL FISIKADocument3 pagesSOAL FISIKAjvsvvblkfdbfboperNo ratings yet
- Aplikasi Gerak Rotasi Pada KatrolDocument5 pagesAplikasi Gerak Rotasi Pada KatrolQonita Nabila HasnaNo ratings yet
- Soal Kimia LombaDocument7 pagesSoal Kimia LombaJoy KarepuNo ratings yet
- Rumus Kimia BatubaraDocument3 pagesRumus Kimia BatubaraRizky AndriawanNo ratings yet
- SIFAT MEKANIK MATERIALDocument25 pagesSIFAT MEKANIK MATERIALnabildamaraNo ratings yet
- Soal Teori Kinetik GasDocument12 pagesSoal Teori Kinetik Gassitti hasnahNo ratings yet
- Induksi MagnetikDocument9 pagesInduksi MagnetikSri Arini RahmawatiNo ratings yet
- ENTALPIDocument37 pagesENTALPIDwyPuspitaSariNo ratings yet
- GELSTASIDocument5 pagesGELSTASIanto hardiNo ratings yet
- Soal Quiz Fluida StatisDocument4 pagesSoal Quiz Fluida StatisAlffredoSihombingNo ratings yet
- 106 153498 Soal2 Latihan Teori Kinetik GasDocument4 pages106 153498 Soal2 Latihan Teori Kinetik GasHanifah Tiara09No ratings yet
- Gelombang StasionerDocument4 pagesGelombang StasionerkorrynilyaniNo ratings yet
- Latihan Soal Us Fisika Kelas Xii 2022Document10 pagesLatihan Soal Us Fisika Kelas Xii 2022mariaNo ratings yet
- Termodinamika IIDocument53 pagesTermodinamika IIsugianto100% (1)
- Konversi SatuanDocument40 pagesKonversi SatuanMitha Al-fauziahNo ratings yet
- Bank Soal Kimia Kelas 11 SMA Bab TermokimiaDocument7 pagesBank Soal Kimia Kelas 11 SMA Bab TermokimiaIstiva Ameilia100% (1)
- Soal Dan Pembahasan Termodinamika SMADocument14 pagesSoal Dan Pembahasan Termodinamika SMAMustariNo ratings yet
- RK13AR11FIS0302Document6 pagesRK13AR11FIS0302Anitaputri ArNo ratings yet
- Materi Fisika SMP Kelas VIIDocument7 pagesMateri Fisika SMP Kelas VIIOket RestouBumi100% (2)
- GetaranDocument23 pagesGetaranMansur Haris100% (2)
- DINAMIKADocument8 pagesDINAMIKARiharsya AllafaNo ratings yet
- TEORI RELATIVITASDocument20 pagesTEORI RELATIVITAScaclubindonesiaNo ratings yet
- KESETIMBANGAN KIMIA RevisiDocument16 pagesKESETIMBANGAN KIMIA RevisiRivellia KumalaNo ratings yet
- Penukar PanasDocument7 pagesPenukar PanasFikri AmirullahNo ratings yet
- Soal Fisika SMADocument9 pagesSoal Fisika SMASiti SyarahNo ratings yet
- Soal CFD Tahun Lalu.Document16 pagesSoal CFD Tahun Lalu.hmpkunmul100% (1)
- Latihan Soal Listrik Statis Xii IpaDocument3 pagesLatihan Soal Listrik Statis Xii IpaGajah Mada100% (1)
- Contoh Soal Penerapan Hukum Kekekalan Energi Mekanik Pada Gerak Di Bidang MiringDocument2 pagesContoh Soal Penerapan Hukum Kekekalan Energi Mekanik Pada Gerak Di Bidang MiringHafid GioNo ratings yet
- Rumus-Rumus TermodinamikaDocument4 pagesRumus-Rumus TermodinamikarhyaninionkNo ratings yet
- Rumus Fisika TermodinamikaDocument11 pagesRumus Fisika TermodinamikaRausan FiqrNo ratings yet
- Bab 7 Marthen KanginanDocument15 pagesBab 7 Marthen KanginanDedi WahyudinNo ratings yet
- Hukum Termodinamika IDocument6 pagesHukum Termodinamika IAyu Marisa Al-RahmanNo ratings yet
- Persamaan Gas Non IdealDocument15 pagesPersamaan Gas Non IdealangelNo ratings yet
- Tugas 2 Termodinamka Xi Ipa2Document4 pagesTugas 2 Termodinamka Xi Ipa2Euis HafsahNo ratings yet
- Hukum TermodinamikaDocument4 pagesHukum TermodinamikaRossollCchcNo ratings yet