Professional Documents
Culture Documents
Kimia Karbon
Uploaded by
Widya WulandariCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Kimia Karbon
Uploaded by
Widya WulandariCopyright:
Available Formats
Kimia Karbon 1. Karbon dan Senyawa karbon Karbon (C) merupakan unsur yang sangat lazim.
Dalam kehidupan sehari-hari kita mengenal beberapa bentuk karbon yaitu arang, grafit, dan intan. Bentuk-bentuk yang berbeda dari unsur yang sama kita kenal dengan istilah alotrop. Perbedaan sifat diantara bentuk alotrop tersebut terjadi karena perbedaan strukturnya. Kelimpahan karbon di kulit bumi hanya sekitar 0,08%. Sekitar 50% dari karbon tersebut terdapat sebagai karbonat, misalnya kalsium karbonat (CaCO3). Selebihnya terdapat sebagai senyawa organic, sebagai karbon dioksida, dan berbagai senyawa karbon lainnya. Hanya sebagian kecil yang terdapat sebagai unsur, yaitu dalam bentuk intan dan arang atau grafit. Walaupun demikian, kabon memegang peranan penting dalam dunia makhluk hidup. Karbon membentuk banyak sekali persenyawaan dan senyawa karbon merupakan pembagian sel hidup. a. Intan Intan adalah zat padat yang bening berkilauan dan merupakan zat yang paling keras. Setiap atom karbon dalam intan berada di pusat suatu tetrahedron dan terikat secara kovalen kepada 4 atom karbon lainnya yang berada di sudut tetrahedron tersebut. Struktur demikian berlanjut ke semua bagian intan membentuk suatu jaringan tiga dimensiyang kokoh dengan titik leleh dan titik didih yang sangat tinggi. Jadi, sebutir intan seberapa pun besarnya merupakan satu molekul raksasa. Penggunaan intan sesuai dngan sifatnya yang keras dan mengkilap. Sebagian besar intan digunakan untuk perhiasan. Intan alam yang tidak cukup baik untuk perhiasan dan intan buatan digunakan untuk membuat alat pemotong (sperti pemotong kaca), gerinda dan mata bor. Intan bubukan digunakan membuat ampelas untuk memoles benda yang sangat keras, seperti baja tahan karat. Intan buatan dibuat dari grafit melalui pemanasan pada suhu sekitar 3300oC dan tekanan 125.000 atm. b. Grafit Grafit mempunyai struktur yang berbentuk lapisan. Dalam satu lapisan, setiap atom karbon terikat secara kovalen kepada 3 atom karbon lainnya, dalam suatu susunan berbentuk heksagonal. Jadi, setiap laipsan adalah satu molekul raksasa. Ikatan antarlapisan jauh lebih lemah dibandingkan dengan ikatan antaratom dalam satu laipsan. Jarak antarlapisan hamper 2,5 kali lebih besar dari jarak antaratom dalam satu lapisan. Hal ini menyebabkan grafit bersifat licin karena satu lapisan dapat
meluncur di atas lapisan lainnya. Hubungan antarlapisan dalam grafit diibaratkan dengan tumpukan lembaran kaca yang basah. Setiap lembaran dapat meluncur di atas lembaran lainnya, tetapi ikatan dalam satu lapisan sangat kuat. Grafit juga mempunyai titik leleh dan titik didih yang sangat tinggi. Dalam grafit, satu elektron terikat agak lemah, sehingga dapat mengalir dari satu atom ke atom lainnya. Oleh karena itu, grafit dapat menghantarkan listrik. Penggunaan grafit terutama berdasarkan sifatnya yang licin dan kemampuannya dalam menghantarkan listrik. Beberapa penggunaan grafit adalah sebagai berikut : 1. Sebagai anode dalam batu baterai dan dalam berbagai proses industri yang menggunakan elektrolisis, misalnya pada peleburan aluminium. 2. Grafit dicampur dengan tanah liat untuk membuat pensil, dan bahan kosmetik. 3. Bahan pelumas. 4. Sebagai komponen dalam pembuatan komposit. Ikatan antaratom karbon dalam setiap lapisan grafit sangat kuat, lebih kuat dari pada baja. Oleh karena itu, serat grafit digunakan untuk membentuk komposit. c. Arang Arang dibuat dari kayu atau serbuk gergaji dengan pemanasan pada suhu tinggi tanpa udara. Arang merupakan kristal halus dengan struktur seperti grafit. Ruang antarlapisan atom dalam arang yang dibubuk halus dapat menyerap (mengadsorpsi) atom atau molekul lain, sehingga zat itu mempunyai daya adsorpsi yang besar. Satu gram arang (karbon aktif), dapat mengadsorpsi 380 ml SO 2 atau 235 ml Cl2 pada suhu kamar, tetapi tidak mengadsorpsi oksigen. Oleh karena itu, bahan ini digunakan dalam topeng gas. Beberapa penggunaan arang yang didasarkan pada sifat adsorpsinya adalah : 1. untuk mengadsorpsi zat warna, dan bahan polutan lainnya pada pengolahan air 2. untuk mengadsorpsi zat warna yang terdapat dalam air tebu pada pengolahan gula 3. sebagai obat sakit perut atau keracunan makanan (norit). d. Karbon Black Karbon black adalah jelaga yang dibuat dari pembakaran hidrokarbon dengan oksigen yang terbatas. Karbon black antara lain digunakan untuk : 1. Vulkanisasi karet pada industri ban 2. membuat ebonite 3. pigmen dala cat, tinta, kertas, dan plastic. e. Karbon Monoksida (CO)
Karbon monoksida (CO) lebih dikenal karena sifatnya yang beracun dari pada kegunaannya. Gas ini dapat berikatan dengan hemoglobin dalam darah sehingga menghalangi fungsi utama darah sebagai pengangkut oksigen. Gas CO tidak berwarna, tidak berbau, dan tidak berasa. Oleh karena itu, tidak ada tanda kehadirannya dan tidak segera dapat disadari. Karbon monoksida di udara berasal dari pembakaran tak sempurna dalam mesin kendaraan bermotor dan industri. Udara bersih praktis tidak mengandung CO. Berikut ini beberapa penggunaan karbon monoksida : 1. sebagai reduktor pada pengolahan berbagai jenis logam, misalnya besi 2. sebagai bahan baku untuk membuat methanol 3. merupakan komponen dari berbagai jenis bahan bakar gas, seperti gas air dan gas kokas. f. Karbon Dioksida (CO2) Berbeda dengan CO, gas CO2 tidak beracun. Akan tetapi, jika kadarnya terlalu besar (10 20%), dapat membuat orang pingsan dan merusak system pernapasan. Walaupun tidak berbau dan tidak berwarna, gas ini mudah dikenali karena mengeruhkan air kapur. Karbon dioksida terdapat di udara dengan kadar sekitar 0,035%. Juga terdapat dalam air, terutama air laut. Karbon dioksida lebih mudah larut dalam air laut karena air laut sedikit bersifat basa, sedangkan CO2 bersifat asam. Karbon dioksida terbentuk pada pembakaran bahan bakar yang mengandung karbon seperti batu bara, minyak bumi, gas alam, dan kayu. Gas ini juga dihasilkan pada pernapasan makhluk hidup. Karbon dioksida merupakan komponen utama siklus karbon di alam. Karbon dioksida komersial diperoleh dari pembakaran residu penyulingan minyak bumi. Dalam jumlah besar juga diperoleh sebagai hasil samping produksi urea dan pembuatan alkohol dari proses peragian. C6H12O6 Glukosa 2C2H5OH + 2CO2 Alkohol
Beberapa penggunaan komersil karbon dioksida adalah sebagai berikut : a. Karbon dioksida mudah dipadatkan. Karbon dioksida padat ini menyublim di bawah tekanan atmosfer (karbon dioksida cair hanya terdapat pada tekanan lebih
besar dari 5,3 atm). Karbon dioksida padat yang disebut es kering (dry ice) digunakan sebagai pendingin. b. Untuk memadamkan kebakaran. Karena CO2 lebih berat dari pada udara, maka CO2 akan memgusir udara dari sekitar daerah yang disemprot sehingga api padam. Tabung pemadam kebakaran berisi CO2 cair dengan tekanan sekitar 60 atm. Ketika katup alat tersebut dibuka maka karbon dioksida cair akan segera menguap dan mengembang. Kedua proses itu menyebabkan penurunan suhu sehingga sebagian CO2 akan membuka membentuk sejenis kabut atau salju yang menutupi daerah yang disemprot. c. Untuk membuat minuman ringan (soft drink). Minuman seperti air soda, limun, dan laiun-lain, mengandung CO2 yang memberi rasa menyegarkan.
You might also like
- Gambar ReprodDocument3 pagesGambar ReprodWidya WulandariNo ratings yet
- Gambar ReprodDocument3 pagesGambar ReprodWidya WulandariNo ratings yet
- Gambar ReprodDocument3 pagesGambar ReprodWidya WulandariNo ratings yet
- 1 SK KD SMP PaiDocument9 pages1 SK KD SMP PaiYwd BaeNo ratings yet
- Materi Pend Islam1Document24 pagesMateri Pend Islam1Widya WulandariNo ratings yet
- Gaya Listrik MuatanDocument1 pageGaya Listrik MuatanWidya WulandariNo ratings yet
- Sebaran Materi Un IpaDocument3 pagesSebaran Materi Un IpaWidya WulandariNo ratings yet
- Pemetaan Ki KD PaiDocument8 pagesPemetaan Ki KD PaiWidya WulandariNo ratings yet
- Soal UN Biologi SMA Tahun 2012Document1 pageSoal UN Biologi SMA Tahun 2012Widya WulandariNo ratings yet
- Soal Essay Biologi CellulairDocument1 pageSoal Essay Biologi CellulairWidya WulandariNo ratings yet
- Peta KonsepDocument3 pagesPeta KonsepWidya WulandariNo ratings yet
- Fakta Menarik TentangDocument3 pagesFakta Menarik TentangWidya WulandariNo ratings yet
- Print Sterilisasi 1Document40 pagesPrint Sterilisasi 1Rini AnggreiniNo ratings yet
- Uji KimiaDocument15 pagesUji KimiaAsty Dewi PangaribuanNo ratings yet
- Analisis PendidikanlidissDocument12 pagesAnalisis PendidikanlidissWidya WulandariNo ratings yet
- Biology 150420230048 Conversion Gate01Document25 pagesBiology 150420230048 Conversion Gate01Widya WulandariNo ratings yet
- SD Kelas 6 - Ilmu Pengetahuan AlamDocument160 pagesSD Kelas 6 - Ilmu Pengetahuan AlamPriyo Sanyoto67% (12)
- Catatan HAM Awal Tahun 2008 - ELSAMDocument24 pagesCatatan HAM Awal Tahun 2008 - ELSAMIndra Jaya Kusuma WardhanaNo ratings yet
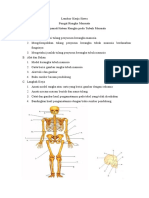
- Fungsi Rangka Manusia (40Document2 pagesFungsi Rangka Manusia (40Widya WulandariNo ratings yet
- Microbiological Examination of Non-Sterile ProductsDocument29 pagesMicrobiological Examination of Non-Sterile ProductsWidya WulandariNo ratings yet
- Implementasi Perlindungan HAM - Adnan Buyung NasutionDocument14 pagesImplementasi Perlindungan HAM - Adnan Buyung NasutionJoko Brantas Lancenk KanakNo ratings yet
- Kurikulum AP SMK N 1 Tampaksiring Edisi 2010Document141 pagesKurikulum AP SMK N 1 Tampaksiring Edisi 2010Widya WulandariNo ratings yet
- Bab 04 Hak Asasi Manusia Dan Penegakkan HukumDocument52 pagesBab 04 Hak Asasi Manusia Dan Penegakkan HukumWidya WulandariNo ratings yet
- Fungsi Rangka Manusia (40Document2 pagesFungsi Rangka Manusia (40Widya WulandariNo ratings yet
- Bab 04 Hak Asasi Manusia Dan Penegakkan HukumDocument52 pagesBab 04 Hak Asasi Manusia Dan Penegakkan HukumWidya WulandariNo ratings yet
- DIURETIK GOLONGAN DAN MEKANISME KERJADocument7 pagesDIURETIK GOLONGAN DAN MEKANISME KERJAYulius Deddy Kristianto25% (4)
- 41HAM Dan Polri NewDocument22 pages41HAM Dan Polri NewMario NicholasNo ratings yet
- Contoh RPP IPA PDFDocument18 pagesContoh RPP IPA PDFWidya WulandariNo ratings yet
- DIURETIK GOLONGAN DAN MEKANISME KERJADocument7 pagesDIURETIK GOLONGAN DAN MEKANISME KERJAYulius Deddy Kristianto25% (4)
- SILABUSDocument1 pageSILABUSWidya WulandariNo ratings yet